摘要:(2)能源的开发,①太阳能:每年辐射到地球表面的能量为5×1019kJ.相当于目前全世界能量消耗的1.3万倍.②生物能:将生物转化为可燃性的液态或气态化合物.再利用燃烧放热.③风能:利用风力进行发电.提水.扬帆助航等技术.风能是一种可再生的干净能源.④地球能.海洋能.
网址:http://m.1010jiajiao.com/timu_id_189411[举报]
(2009?四川)新型锂离子电池在新能源的开发中占有重要地位,可用作节能环保电动汽车的动力电池.磷酸亚铁锂(LiFePO4)是新型锂离子电池的首选电极材料,它的制备方法如下:
方法一:将碳酸锂、乙酸亚铁[(CH3COO)2Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出.
方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀.沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂.
在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:
请回答下列问题:
(1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行.其原因是
(2)在方法一所发生的反应中,除生成磷酸亚铁锂、乙酸外,还有
(3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为
(4)写出M与足量氢氧化钠溶液反应的化学方程式:
 .
.
(5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为
查看习题详情和答案>>
方法一:将碳酸锂、乙酸亚铁[(CH3COO)2Fe]、磷酸二氢铵按一定比例混合、充分研磨后,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂,同时生成的乙酸及其它产物均以气体逸出.
方法二:将一定浓度的磷酸二氢铵、氯化锂混合溶液作为电解液,以铁棒为阳极,石墨为阴极,电解析出磷酸亚铁锂沉淀.沉淀经过滤、洗涤、干燥,在800℃左右、惰性气体氛围中煅烧制得晶态磷酸亚铁锂.
在锂离子电池中,需要一种有机聚合物作为正负极之间锂离子迁移的介质,该有机聚合物的单体之一(用M表示)的结构简式如下:

请回答下列问题:
(1)上述两种方法制备磷酸亚铁锂的过程都必须在惰性气体氛围中进行.其原因是
为了防止亚铁化合物被氧化
为了防止亚铁化合物被氧化
.(2)在方法一所发生的反应中,除生成磷酸亚铁锂、乙酸外,还有
CO2
CO2
、H2O
H2O
、NH3
NH3
(填化学式)生成.(3)在方法二中,阳极生成磷酸亚铁锂的电极反应式为
Fe+H2PO4-+Li+-2e-=LiFePO4+2H+
Fe+H2PO4-+Li+-2e-=LiFePO4+2H+
.(4)写出M与足量氢氧化钠溶液反应的化学方程式:


(5)已知该锂离子电池在充电过程中,阳极的磷酸亚铁锂生成磷酸铁,则该电池放电时正极的电极反应式为
FePO4+Li++e-═LiFePO4
FePO4+Li++e-═LiFePO4
. 能源的开发利用与人类社会的可持续性发展息息相关.
能源的开发利用与人类社会的可持续性发展息息相关.I已知:Fe2O3(s)+3C(s)=2Fe(s)+3CO(g)△H1=akJ?mol-1
CO(g)+
| 1 |
| 2 |
4Fe(s)+3O2(g)=2Fe2O3(s)△H3=ckJ?mol-1
则C的燃烧热
II(I)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
A.C(s)+C02(g)=2C0(g)
B.Na0H(aq)+HCl(aq)=NaCl(aq)+H20(1)
C.2H20(l)=2H2(g)+02(g)
D.2C0(g)+02(g)=2C02(g)
若以熔融的K2CO3与CO2为反应的环境,依据所选反应设计成一个原电池,诸写出该原电池的负极反应:
(2)某实验小组模拟工业合成氨反应N2+3H2
| 高温、高压 |
| 催化剂 |
| P |
| P0 |
①反应达平衡的标志是(填字母代号)
A.压强保持不变
B.气体密度保持不变
C.NH3的生成速率是N2的生成速率的2倍
②2min时,以C(N2)变化表示的平均反应速率为
③若提高N2的转化率可采取的措施有
A.向体系中按体积比1:1再充入N2和H2 B.分离出NH3
C.升高温度 D.充入He气使压强增大 E.加入一定量的N2
(3)25°C时,BaCO3和BaSO4的溶度积常数分别是8×10-9和1×10-10,某含有BaCO3沉淀的悬浊液中,c(C
| O | 2- 3 |
随着化石能源的减少,新能源的开发利用日益迫切.
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
SO2(g)+I2(g)+2H2O(g)=2HI (g)+H2SO4(l)△H=a kJ?mol-1
2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g)△H=b kJ?mol-1
2HI(g)=H2(g)+I2(g)△H=c kJ?mol-1
则:2H2O(g)=2H2(g)+O2(g)△H= kJ?mol-1
(2)甲醇制氢有以下三个反应:
CH3OH(g)=CO(g)+2H2(g)△H=+90.8kJ?mol-1 Ⅰ
CO(g)+H2O(g)=CO2(g)+H2(g)△H=-43.5kJ?mol-1 Ⅱ
CH3OH(g)+
O2(g)=CO2(g)+2H2(g)△H=-192.0kJ?mol-1 Ⅲ
①当CH3OH(g)、O2(g)、H2O(g)总进料量为1mol时,且n(CH3OH):n(H2O):n(O2)=0.57:0.28:0.15,在0.1MPa、473~673K温度范围内,各组分的平衡组成随温度变化的关系曲线见图.(图中Yi表示各气体的体积分数,氧气的平衡浓度接近0,图中未标出).下列说法正确的是 .
A.在0.1MPa、473~673K温度范围内,甲醇有很高的转化率
B.温度升高有利于氢气的制备
C.寻找在较低温度下的催化剂在本制氢工艺中至关重要
②已知反应Ⅱ在T1℃时K=1,向恒容的密闭容器中同时充入1.0mol CO、3.0molH2O,达到平衡时CO的转化率为 .在反应达到平衡后再向其中加入1.0mol CO、1.0mol H2O、1.0mol CO2和1.0mol H2,此时该反应的v正 v逆(填“>”、“<”或“=”).
(3)一种以甲醇作燃料的电池示意图见图.写出该电池放电时负极的电极反应式: .
(4)LiBH4有很高的燃烧热,可做火箭的燃料,写出其燃烧反应的化学方程式: .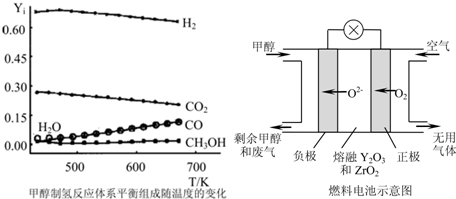
查看习题详情和答案>>
(1)Bunsen热化学循环制氢工艺由下列三个反应组成:
SO2(g)+I2(g)+2H2O(g)=2HI (g)+H2SO4(l)△H=a kJ?mol-1
2H2SO4(l)=2H2O(g)+2SO2(g)+O2(g)△H=b kJ?mol-1
2HI(g)=H2(g)+I2(g)△H=c kJ?mol-1
则:2H2O(g)=2H2(g)+O2(g)△H=
(2)甲醇制氢有以下三个反应:
CH3OH(g)=CO(g)+2H2(g)△H=+90.8kJ?mol-1 Ⅰ
CO(g)+H2O(g)=CO2(g)+H2(g)△H=-43.5kJ?mol-1 Ⅱ
CH3OH(g)+
| 1 | 2 |
①当CH3OH(g)、O2(g)、H2O(g)总进料量为1mol时,且n(CH3OH):n(H2O):n(O2)=0.57:0.28:0.15,在0.1MPa、473~673K温度范围内,各组分的平衡组成随温度变化的关系曲线见图.(图中Yi表示各气体的体积分数,氧气的平衡浓度接近0,图中未标出).下列说法正确的是
A.在0.1MPa、473~673K温度范围内,甲醇有很高的转化率
B.温度升高有利于氢气的制备
C.寻找在较低温度下的催化剂在本制氢工艺中至关重要
②已知反应Ⅱ在T1℃时K=1,向恒容的密闭容器中同时充入1.0mol CO、3.0molH2O,达到平衡时CO的转化率为
(3)一种以甲醇作燃料的电池示意图见图.写出该电池放电时负极的电极反应式:
(4)LiBH4有很高的燃烧热,可做火箭的燃料,写出其燃烧反应的化学方程式:

下列关于能源的说法,正确的有几个( )
①能源就是能提供能量的资源;
②能源的开发和利用可衡量一个国家或地区的经济发展和科学技术水平;
③我国目前使用的主要能源是化石燃料,但其缺点明显,如储量有限、不可再生、有污染等;
④解决能源危机的有效办法包括提高能源利用率、寻找新能源等.
①能源就是能提供能量的资源;
②能源的开发和利用可衡量一个国家或地区的经济发展和科学技术水平;
③我国目前使用的主要能源是化石燃料,但其缺点明显,如储量有限、不可再生、有污染等;
④解决能源危机的有效办法包括提高能源利用率、寻找新能源等.
查看习题详情和答案>>
能源的开发、利用与人类社会的可持续发展息息相关,怎样充分利用好能源是摆在人类面前的重大课题.
I.已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H=akJ?mol-1
CO(g)+1/2O2(g)=CO2(g)△H=bkJ?mol-1
C(石墨)+O2(g)=CO2(g)△H=ckJ?mol-1
则反应:4Fe(s)+3O2(g)=2Fe2O3(s)的焓变△H=
Ⅱ.(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
A.C(s)+CO2(g)=2CO(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2H2O(l)=2H2(g)+O2(g)
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l)
若以KOH溶液为电解质溶液,依据所选反应可以设计成一个原电池,请写出该原电池的电极反应.
负极:
正极:
(2)二氧化氯(ClO2)是一种高效安全的自来水消毒剂.ClO2是一种黄绿色气体,易溶于水.实验室以NH4Cl、盐酸、NaClO2为原料制备ClO2流程如下:

已知:电解过程中发生的反应为:
NH4Cl+2HCl
NCl3+3H2↑;假设NCl3中氮元素为+3价.
①写出电解时阴极的电极反应式
②在阳极上放电的物质(或离子)是
③除去ClO2中的NH3可选用的试剂是
A.生石灰 B.碱石灰 C.浓H2SO4 D.水
④在生产过程中,每生成1mol ClO2,需消耗
mol NCl3.
查看习题详情和答案>>
I.已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H=akJ?mol-1
CO(g)+1/2O2(g)=CO2(g)△H=bkJ?mol-1
C(石墨)+O2(g)=CO2(g)△H=ckJ?mol-1
则反应:4Fe(s)+3O2(g)=2Fe2O3(s)的焓变△H=
6(c-b)-2a
6(c-b)-2a
kJ?mol-1.Ⅱ.(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
D
D
(填序号).A.C(s)+CO2(g)=2CO(g)
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)
C.2H2O(l)=2H2(g)+O2(g)
D.CH4(g)+2O2(g)=CO2(g)+2H2O(l)
若以KOH溶液为电解质溶液,依据所选反应可以设计成一个原电池,请写出该原电池的电极反应.
负极:
CH4-8e-+10OH-=CO32-+7H2O
CH4-8e-+10OH-=CO32-+7H2O
,正极:
O2+2H2O+4e-=4OH-
O2+2H2O+4e-=4OH-
.(2)二氧化氯(ClO2)是一种高效安全的自来水消毒剂.ClO2是一种黄绿色气体,易溶于水.实验室以NH4Cl、盐酸、NaClO2为原料制备ClO2流程如下:

已知:电解过程中发生的反应为:
NH4Cl+2HCl
| ||
. |
①写出电解时阴极的电极反应式
2H++2e-=H2↑
2H++2e-=H2↑
.②在阳极上放电的物质(或离子)是
NH4Cl(NH4+)
NH4Cl(NH4+)
.③除去ClO2中的NH3可选用的试剂是
C
C
(填序号)A.生石灰 B.碱石灰 C.浓H2SO4 D.水
④在生产过程中,每生成1mol ClO2,需消耗
| 1 |
| 6 |
| 1 |
| 6 |