摘要:进行中和热实验测定时.需要测定反应前盐酸和氢氧化钠溶液的温度及反应后溶液的最低温度解析:正确的做法是需要测定反应前盐酸和氢氧化钠溶液的温度及反应后溶液的最高温度.
网址:http://m.1010jiajiao.com/timu_id_189371[举报]
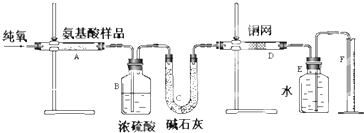
中和热的测定实验的关键是要较准确地配制一定物质的量浓度的溶液,量热器要尽量做到绝热;在量热过程中要尽量避免热量的散失,要求比较准确地测量出反应前后溶液温度的变化.完成下列问题.
(1)中和热的测定所需的玻璃仪器有:大小烧杯,量筒2个,________,________;结合日常生活,该实验可以改在________(一生活用品)中进行.
(2)该实验常用0.50 mol/L HCl和0.55 mol/L的NaOH溶液各50 mL.NaOH溶液浓度大于HCl的浓度的作用是________.当室温低于10℃时进行,对实验结果会造成较大的误差,其原因是________.
测定硫酸铜晶体(CuSO4?5H2O)里结晶水的含量,实验步骤为:①研磨 ②称量空坩埚和装有试样的坩埚的质量 ③加热 ④冷却 ⑤称量 ⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止 ⑦根据实验数据计算硫酸铜结晶水的含量.
请回答下列问题:
(1)现有坩埚、坩埚钳、三脚架、泥三角、玻璃棒、干燥器、药匙、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是
(2)该实验中哪一步骤需要使用干燥器?使用干燥器的目的是什么?
答:
(3)实验步骤⑥的目的是
(4)若操作正确而实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有(填入选项的编号):
A.被测样品中含有加热不挥发的杂质
B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水
D.加热前所用的坩埚未完全干燥.
查看习题详情和答案>>
请回答下列问题:
(1)现有坩埚、坩埚钳、三脚架、泥三角、玻璃棒、干燥器、药匙、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品是
研钵、托盘天平、酒精灯
研钵、托盘天平、酒精灯
.(2)该实验中哪一步骤需要使用干燥器?使用干燥器的目的是什么?
答:
冷却
冷却
.(3)实验步骤⑥的目的是
检验样品中的结晶水是否已经全部除去
检验样品中的结晶水是否已经全部除去
.(4)若操作正确而实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有(填入选项的编号):
A、C
A、C
.A.被测样品中含有加热不挥发的杂质
B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水
D.加热前所用的坩埚未完全干燥.
实验室需要0.1mol?L-1NaOH溶液450mL和0.5mol?L-1硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是

(2)容量瓶不能用于
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为
(4)根据计算得知,所需质量分数为98%、密度为1.84g?cm-3的浓硫酸的体积为
查看习题详情和答案>>
(1)如图所示的仪器中配制溶液肯定不需要的是
AC
AC
(填序号),配制上述溶液还需用到的玻璃仪器是烧杯和玻璃棒
烧杯和玻璃棒
(填仪器名称).
(2)容量瓶不能用于
BCF
BCF
(填序号).A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.准确稀释某一浓度的溶液
E.量取一定体积的液体
F.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为
2.0
2.0
g.在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度小于
小于
0.1mol?L-1(填“大于”“等于”或“小于”,下同).若NaOH溶液在转移至容量瓶时,洒落了少许,则所得溶液浓度小于
小于
0.1mol?L-1.(4)根据计算得知,所需质量分数为98%、密度为1.84g?cm-3的浓硫酸的体积为
13.6
13.6
mL(计算结果保留一位小数).如果实验室有15mL、20mL、50mL量筒,应选用15
15
mL量筒最好.配制过程中需先在烧杯中将浓硫酸进行稀释,稀释时操作方法是将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌
将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌
.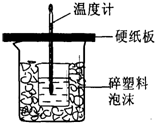 实验室用50mL0.50mol/L盐酸、50mL0.50mol/LNaOH溶液和如图所示装置进行测定中和热的实验,得到表中的数据:
实验室用50mL0.50mol/L盐酸、50mL0.50mol/LNaOH溶液和如图所示装置进行测定中和热的实验,得到表中的数据:| 实验次数 |
起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
环形玻璃搅拌棒
环形玻璃搅拌棒
;实验时用该仪器搅拌溶液的方法是上下搅动
上下搅动
,由图可知该装置有不妥之处,应如何改正?应使小烧杯口与大烧杯口持平,其余部分用碎塑料填满
应使小烧杯口与大烧杯口持平,其余部分用碎塑料填满
.(2)反应需要多次测量温度,每次测量温度后都必须采取的操作是
用水将温度计上的液体冲掉,并擦干温度计
用水将温度计上的液体冲掉,并擦干温度计
.(3)已知Q=cm△t,经数据处理,则该实验测得的中和热△H=
-56.8kJ/mol
-56.8kJ/mol
(盐酸和NaOH溶液的密度按1g/cm3计算,反应后混合溶液的比热容(c)按4.18J/(g?℃)计算).
(4)盐酸与氢氧化钠的中和热的文献值为-57.3kJ/mol,你认为(3)中测得的实验值偏差可能的原因是
①量热计的保温瓶绝热效果不好 ②酸碱溶液混合不迅速
①量热计的保温瓶绝热效果不好 ②酸碱溶液混合不迅速
(至少说出两点)(5)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热为△H1,则△H1与△H的关系为:△H1
>
>
△H(填“<”、“>”或“=”),理由是NH3?H2O电离吸热
NH3?H2O电离吸热
.