网址:http://m.1010jiajiao.com/timu_id_189293[举报]
(1)配平第①步反应的离子方程式:
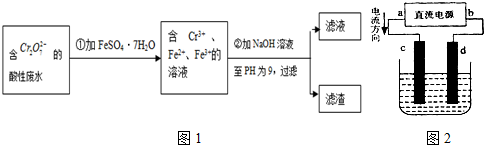
(2)设计一个电解装置也可以实现上述目的,装置如图2(用铁棒和石墨作电极):
电极材料c为:
d极电极反应为:
(3)已知:25℃时Ag2Cr2O7的Ksp=2×10-7.则25℃时,将4×10-2mol?L-1的AgNO3溶液与4×10-4mol?L-1的K2Cr2O7溶液等体积混合
(Ⅰ)2SO2(g)+O2(g)  2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。请回答下列问题:
(1)图中A表示 。
(2)E的大小对该反应的焓变有无影响? 。
该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低? 。
(3)某温度下,向1L密闭容器中开始充入2molSO2和1molO2,在V2O5催化剂存在时反应达到平衡,压强减小为开始时的 ;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g)
;如在相同温度下,在同等体积的密闭容器中充入2mol的SO3,也在V2O5催化剂存在时反应达到平衡,求此温度下反应2SO3 (g)  2SO2(g) + O2(g)的平衡常数(写出计算过程)
2SO2(g) + O2(g)的平衡常数(写出计算过程)
(Ⅱ)化学试剂的生产和电镀工业排放的废水中常含有20~100mg.L-1Cr(Ⅵ),饮用含Cr(Ⅵ)的水会损害人的肠胃等,已知Cr(Ⅲ)的毒性是Cr(Ⅵ)的0.5%,国家规定工业废水含Cr(Ⅵ)的量排放标准为0.1mg.L-1。工业上常用化学法和电解法处理含Cr(Ⅵ)废水,再将Cr(Ⅲ)转化成沉淀除去,某研究性学习小组为研究废水的净化,设计了如下实验流程:
(1)配平第①步反应的离子方程式:
(2)第②步中用PH试纸测定溶液PH的操作是:
(3)设计一个电解装置也可以实现上述目的,装置如下图(用铁棒和石墨作电极):
电极材料:c为:
电极反应:d极:
假如你是一位企业家,在众多开发海水资源的项目中,选择了海水提镁,在前期考察过程中你将遇到许多问题,请根据背景材料的提示,按要求完成相关问题:
背景材料1:下面所示为海水中各元素含量情况(mg/L)
|
元素 |
浓度(mg/L) |
元素 |
浓度(mg/L) |
|
钠 |
10 770 |
氯 |
19 350 |
|
镁 |
1 290 |
硫 |
885 |
|
钾 |
380 |
溴 |
67 |
|
钙 |
400 |
碘 |
0.06 |
背景材料2:部分化学试剂的市场价格
|
试剂 |
氢氧化钾 |
氢氧化钠 |
氢氧化钙 |
氧化钙 |
|
价格(元/吨) |
5 238.00 |
2 300.00 |
1 200.00 |
700.00 |
请完成下列问题:
(1)在海水提镁的过程中要实现对镁离子的富集、分离,有以下三个方案:
方案一:直接往海水中加入沉淀剂;
方案二:加热蒸发海水再加入沉淀剂;
方案三:在晒盐后的卤水中加入沉淀剂。
你认为方案________最合理。
不选方案________的理由是________________________________________________
不选方案________的理由是_______________________________________________
(2)应该选择________试剂作为镁离子的沉淀剂。不考虑其他费用,沉淀相同量的镁离子所用氢氧化钠和氧化钙的价格比为________。
(3)为了节省成本,考虑以海边上的贝壳为原料,试简述其理由__________________________
查看习题详情和答案>>


A.烧杯 B.表面皿 C.蒸发皿 D.坩埚 E.试管 .酒精灯 G.泥三角
(2) 将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式 ___________________________。
(3) 操作①的名称是________;试剂A为________(填本题表格中一种最佳化学试剂的名称),不使用另外两种试剂的主要原因分别是: ①_____________________; ②_______________________。
(4) 操作②中所用的主要玻璃仪器为________,振荡、静置,应首先将________分离出来。
(5) 将下列装置图中缺少的必要仪器补画出来以最终将单质碘与试剂A分离

