摘要:4.在银镜反应配制银氨溶液时.稀氨水与稀硝酸银溶液的滴加顺序.相对量的控制.描述时必须注意.五.有机物除杂常见错误及原因分析依据有机物的水溶性.互溶性以及酸碱性等.可选择不同的分离方法达到分离.提纯的目的.在进行分离操作时.通常根据有机物的沸点不同进行蒸馏或分馏,根据物质的溶解性不同.采取萃取.结晶或过滤的方法.有时也可以用水洗.酸洗或碱洗的方法进行提纯操作.下面就有机物提纯中常见的错误操作进行分析.
网址:http://m.1010jiajiao.com/timu_id_189251[举报]
| A.银镜反应实验后附有银的试管,可用稀H2SO4清洗 |
| B.在中学《硫酸铜晶体里结晶水含量测定》的实验中,称量操作至少需要四次 |
| C.不慎将浓硫酸沾在皮肤上,立即用NaOH溶液冲洗 |
| D.配制FeCl3溶液时,将FeCl3固体溶于较浓盐酸中,然后再用水稀释到所需的浓度 |
F.不慎接触过多的氨,及时吸人新鲜的空气和水蒸气,并用大量水冲洗眼睛
化学实验中常将溶液或试剂进行酸化或碱化,下列处理方法正确的是( )
| A.检验C2H5Cl中的氯元素时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸进行酸化 |
| B.为了提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液进行酸化 |
| C.鉴别待测液是否含有Fe2+时,用HNO3酸化 |
| D.进行乙醛银镜反应时,常在新配制的银氨溶液中,滴入少量稀NaOH溶液 |
化学实验中常将溶液或试剂进行酸化或碱化,下列处理方法正确的是
- A.检验C2H5Cl中的氯元素时,将C2H5Cl和NaOH溶液混合加热后,加入稀硫酸进行酸化
- B.为了提高KMnO4溶液的氧化能力,用盐酸将KMnO4溶液进行酸化
- C.鉴别待测液是否含有Fe2+时,用HNO3酸化
- D.进行乙醛银镜反应时,常在新配制的银氨溶液中,滴入少量稀NaOH溶液
(1)在焊接铜漆包线的线头时,常先把线头放在火上烧一下,以除去漆层,并立即在酒精中蘸一下,再焊接.为什么要用酒精处理后再焊接,试用化学方程式来说明:
(2)现用硝酸银溶液和氨水配制银氨溶液,请简述配制过程:
(3)写出乙醛发生银镜反应的化学方程式:
(4)做过银镜实验的试管,可以用下列
A.稀硝酸 B.稀盐酸 C.稀硫酸 D.硫酸铜溶液.
查看习题详情和答案>>
2Cu+O2
2CuO,CuO+CH3CH2OH
Cu+CH3CHO+H2O
| ||
| ||
2Cu+O2
2CuO,CuO+CH3CH2OH
Cu+CH3CHO+H2O
.
| ||
| ||
(2)现用硝酸银溶液和氨水配制银氨溶液,请简述配制过程:
在洁净的试管中加入1mL2%的硝酸银溶液,边振荡边逐滴加入2%的稀氨水,至最初产生的白色沉淀恰好溶解为止,制得银氨溶液
在洁净的试管中加入1mL2%的硝酸银溶液,边振荡边逐滴加入2%的稀氨水,至最初产生的白色沉淀恰好溶解为止,制得银氨溶液
.(3)写出乙醛发生银镜反应的化学方程式:
CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag+3NH3+H2O
| △ |
CH3CHO+2Ag(NH3)2OH
CH3COONH4+2Ag+3NH3+H2O
.| △ |
(4)做过银镜实验的试管,可以用下列
A
A
试剂进行清洗(填序号).A.稀硝酸 B.稀盐酸 C.稀硫酸 D.硫酸铜溶液.
(1)下列叙述完全正确的是______________(填序号)。
A.测溶液pH的方法是:取一小片广泛pH试纸置于玻璃片或表面皿上,再用干燥、洁净的玻璃棒蘸取溶液,点在pH试纸中部,然后跟标准比色卡比较
B.在测定硫酸铜晶体结晶水含量的实验中,下列操作都会导致测定结果偏高:①加热前称量容器时,容器未完全干燥 ②加热过程中有少量晶体溅出 ③加热后容器未放入干燥器中冷却
C.配制0.1 mol·L-1的NaCl溶液250 mL,烧杯、玻璃棒、250 mL的容量瓶、胶头滴管等玻璃仪器必须用到
D.用50 mL酸式滴定管量取25.00 mL稀盐酸的操作可以是:先将稀盐酸注入酸式滴定管,调节其凹液面正好与25 mL该度相切,然后将溶液全部放入50 mL锥形瓶中
E.硝酸钾溶解度测定的实验中,温度计的水银球应处于烧杯中的水浴液面以下;分馏石油时,温度计的水银球应处于蒸馏烧瓶的支管口处
F.仪器洗涤中常采用下列方法:①用酒精清洗制取酚醛树脂用过的大试管 ②用氨水清洗做过银镜反应的试管 ③用浓盐酸稍加热清洗用高锰酸钾制氧气后的试管
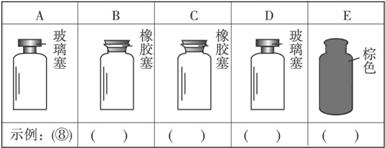
(2)实验室里化学试剂的保存方法是不相同的,下图中A、B、C、D、E是常见的一些保存药品的试剂瓶。请把下列常见试剂的序号填写在各试剂瓶下方的括号里:
①浓硫酸 ②碳酸钾溶液 ③碱石灰 ④四氯化碳 ⑤氯水 ⑥浓硝酸 ⑦硝酸银溶液 ⑧金属钠