摘要:(5)“ 是①醇消去H2O生成烯烃或炔烃,②酯化反应,③纤维素的水解反应,
网址:http://m.1010jiajiao.com/timu_id_189212[举报]
(2010?南开区二模)A、B、C、D、E、F、G、H、I、J均为有机化合物.根据框图所示,回答问题.

(1)B和C均为有支链的有机化合物,B的结构简式为
(2)F所含官能团的名称是
(3)G能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式为:
(4)写出下列反应的化学方程式:
反应⑤
 .
.
反应⑨
 .
.
(5)写出下列反应的反应类型:
反应①
(6)写出与H具有相同官能团的H的同分异构体的所有可能的结构:
 .
.
查看习题详情和答案>>

(1)B和C均为有支链的有机化合物,B的结构简式为
(CH3)2CHCOOH
(CH3)2CHCOOH
,C在浓硫酸作用下加热反应只能生成一种烯烃D,D的结构简式为(CH3)2C=CH2
(CH3)2C=CH2
.(2)F所含官能团的名称是
醇羟基、碳碳双键
醇羟基、碳碳双键
.(3)G能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式为:
CH2=C(CH3)-CHO
CH2=C(CH3)-CHO
.(4)写出下列反应的化学方程式:
反应⑤


反应⑨


(5)写出下列反应的反应类型:
反应①
水解反应
水解反应
、反应③消去反应
消去反应
、反应⑦氧化反应
氧化反应
.(6)写出与H具有相同官能团的H的同分异构体的所有可能的结构:


已知:A、D、E、X、Y、Z是原子序数依次增大的短周期主族元素.A能形成密度最小的气体单质,D元素某种单质的硬度最大,X是地壳中含量最多的元素,Y的气态氢化物有臭鸡蛋气味,其氧化物能使品红溶液褪色,H、W是常见金属,其元素的含量分别位于地壳中金属元素含量的第一、第二位.
(1)W元素在周期表中的位置为 ;H能与具有磁性的W的化合物发生反应,在工业上有重要应用.写出该反应的化学方程式 .
(2)A、E两种元素组成的某种气体分子,一个分子中含有10个电子,实验室制取该气体的化学反应方程式为: .
(3)甲由A、E两种元素组成,分子中含有18个电子,只存在共价单键,常温下甲是一种无色液体.甲在碱性溶液中能够将CuO还原为CH2O,已知当1mol甲完全参加反应时转移了4mol电子,则该反应的化学方程式可表示为: .
(4)处理含DX、YX2烟道气污染的一种方法,是在催化剂作用下使两者反应,产物之一为单质Y.已知反应生成1gY固体单质时放出8.4kJ热量.此反应的热化学方程式为 .
(5)由钠和X、Z三种元素组成的一种阴、阳离子个数之比为1:1的化合物乙,是84消毒液的主要成分,其溶液显碱性,原因是 .(用离子方程式表示)该化合物所含的化学键类型有 .
(6)已知:W3+的浓度为0.04mol/L,室温下W(OH)3的Ksp=4×10-38,要使W3+开始形成沉淀的最小pH是 .
查看习题详情和答案>>
(1)W元素在周期表中的位置为
(2)A、E两种元素组成的某种气体分子,一个分子中含有10个电子,实验室制取该气体的化学反应方程式为:
(3)甲由A、E两种元素组成,分子中含有18个电子,只存在共价单键,常温下甲是一种无色液体.甲在碱性溶液中能够将CuO还原为CH2O,已知当1mol甲完全参加反应时转移了4mol电子,则该反应的化学方程式可表示为:
(4)处理含DX、YX2烟道气污染的一种方法,是在催化剂作用下使两者反应,产物之一为单质Y.已知反应生成1gY固体单质时放出8.4kJ热量.此反应的热化学方程式为
(5)由钠和X、Z三种元素组成的一种阴、阳离子个数之比为1:1的化合物乙,是84消毒液的主要成分,其溶液显碱性,原因是
(6)已知:W3+的浓度为0.04mol/L,室温下W(OH)3的Ksp=4×10-38,要使W3+开始形成沉淀的最小pH是
从2011年5月1日起,醉酒驾驶将作为危险驾驶罪被追究驾驶人刑事责任.已知有两种酶与酒精的代谢有关,一种是醇脱氢酶(ADH),另一种是醛脱氢酶(ALDH),则此两种酶应属于( )
查看习题详情和答案>>
(2009?徐汇区二模)已知:
芳香烃A能发生下面一系列化学反应:
请回答下列问题:
(1)写出下列物质的结构简式:G
 ,A
,A
 ;
;
(2)写出下列反应的反应类型:②
(3)书写下列反应的化学方程式:
①

⑤

(4)上述流程中的物质,互为同分异构体的是
(5) 是制造集成电路不可缺少的物质,其单体可以通过G与乙炔加成制得.写出反应的化学方程式
是制造集成电路不可缺少的物质,其单体可以通过G与乙炔加成制得.写出反应的化学方程式
 .
.
查看习题详情和答案>>

芳香烃A能发生下面一系列化学反应:

请回答下列问题:
(1)写出下列物质的结构简式:G




(2)写出下列反应的反应类型:②
取代
取代
,③氧化
氧化
,⑥消去
消去
;(3)书写下列反应的化学方程式:
①


⑤


(4)上述流程中的物质,互为同分异构体的是
C与G
C与G
(填编号);(5)
 是制造集成电路不可缺少的物质,其单体可以通过G与乙炔加成制得.写出反应的化学方程式
是制造集成电路不可缺少的物质,其单体可以通过G与乙炔加成制得.写出反应的化学方程式

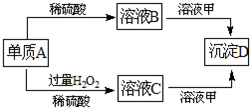 (2011?潍坊模拟)A、B、C、D和甲有以下转化关系.已知物质甲是短周期元素组成的盐,且是某种消毒液的有效成分,沉淀D可溶于酸.请回答下列问题:
(2011?潍坊模拟)A、B、C、D和甲有以下转化关系.已知物质甲是短周期元素组成的盐,且是某种消毒液的有效成分,沉淀D可溶于酸.请回答下列问题:(1)组成A的元素在周期表中位于第
四
四
周期第Ⅷ
Ⅷ
族.(2)鉴定C中阳离子(不考虑H+)的操作和现象是
取少量C溶液于试管中,滴入KSCN溶液,溶液显红色,说明C中有Fe3+离子
取少量C溶液于试管中,滴入KSCN溶液,溶液显红色,说明C中有Fe3+离子
.(3)A转化为B时会放出无色气体E,在298K时1mol A完全反应放出热量QkJ,则该反应的热化学方程式为
Fe(s)+2H+ (aq)=Fe2+(aq)+H2(g);△H=-QkJ/mol
Fe(s)+2H+ (aq)=Fe2+(aq)+H2(g);△H=-QkJ/mol
.(4)若A转化为C时无气体放出,写出该反应的化学方程式:
2Fe+3H2O2+3H2SO4=Fe2(SO4)3+6H2O
2Fe+3H2O2+3H2SO4=Fe2(SO4)3+6H2O
.(5)写出溶液C和溶液甲反应的离子方程式:
Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO
Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO
.