网址:http://m.1010jiajiao.com/timu_id_189173[举报]
已知:①SO2难溶于饱和亚硫酸氢钠溶液.②SO2能与酸性高锰酸钾溶液发生氧化还原反应.
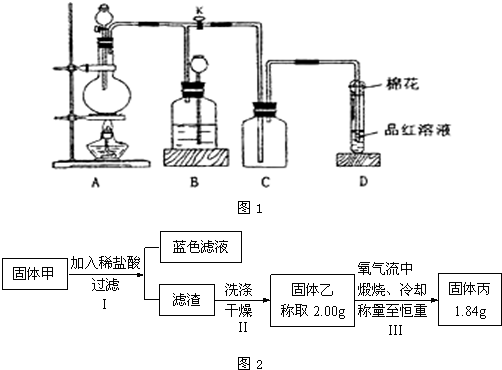
请回答:
(1)装置A中发生的化学反应方程式为
| ||
| ||
a.酸性 b.脱水性 c.强氧化性 d.吸水性
(2)装置D中试管口放置的棉花中浸入
(3)装置B的作用是贮存多余的气体.当D处有明显的现象后,关闭旋塞K并移去酒精灯,但由于余热的作用,A处仍有气体产生,此时B中的现象是
a.水 b.饱和NaHSO3溶液 c.酸性KMnO4溶液 d.NaOH溶液
(4)实验中,取一定质量的铜片和一定体积18.4mol?L-1的浓硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余.
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②下列药品中能用来证明反应结束后的烧瓶中确有余酸的是(填字母)
a.银粉 b.铁粉 c.BaCl2溶液 d.NaHCO3溶液
(5)实验中发现试管内除了产生白色固体外,在铜表面还产生黑色固体甲,其中可能含有氧化铜、硫化铜、硫化亚铜,以及被掩蔽的氧化亚铜.
查阅资料:
i.氧化亚铜在酸性环境下会发生自身氧化还原反应生成Cu2+和铜单质,在氧气流中煅烧,可以转化为氧化铜.
ii.硫化铜和硫化亚铜常温下都不溶于稀盐酸,在氧气流中煅烧,硫化铜和硫化亚铜都转化为氧化铜和二氧化硫.
为了研究甲的成分,该小组同学在收集到足够量的固体甲后,进行了如图2所示实验:
①Ⅲ中在煅烧过程中一定发生的反应的化学方程式为
| ||
| ||
②下列对于固体甲的成分的判断中,正确的是(填字母选项)
a.固体甲中,CuO和Cu2O至少有一种
b.固体甲中,CuS和Cu2S不能同时存在
c.固体甲中若没有Cu2O,则一定有Cu2S
d.固体甲中若存在Cu2O,也可能有Cu2S.
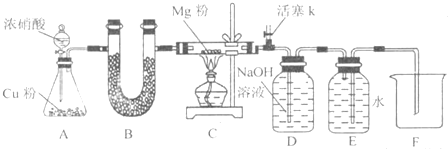
I.同体产物为MgO.
II.假设为
III.假设为:
请回答下列问题:
资料信息:2N02+2NaOH=NaNO3+NaNO2+H2O
(1)如图连接好仪器,装药品前如何检验装置的气密性
(2)装置B中盛装的干燥剂可以是(填序号)
①浓硫酸②无水CaCl2③碱心灰④五氧化二磷
(3)开始打开活塞k,让A中反应进行一段时间,待C中充满红综色气体后,关闭 活塞k,再点燃C处酒精灯,同时D中碱液盛的很满,这样做的H的都是
(4)E中收集到的气体对氢气的相对密度是14,该气体是
(5)实验得到阀体残留物的质量是实验前Mg粉质铽的1.5倍,则假设
(6)本实验中存在明显缺陷,改进措施是
某实验小组欲测定KMnO4的分解率α,但加热前忘记称量KMnO4的质量。面对此情况,甲同学采用下述方法:在加热时,利用浓盐酸与KMnO4受热部分分解后所得的固体混合物反应产生的Cl2被碱石灰吸收,通过碱石灰增重来计算KMnO4的分解率α。(与热的浓盐酸反应时,固体混合物中的Mn元素均被还原成Mn2+)

取KMnO4受热部分分解后所得的固体混合物mg进行实验,请从k@s^5*u上图中选用所需的仪器(可重复选用)组成一套反应装置,其它固、液试剂自选。(其中某些连接和固定仪器用的
玻璃管、胶管、铁夹、铁架台及加热装置、打气筒等均略去)
(1)在反应发生前,为了消除装置内空气中酸性气体的影响,须用打气筒向装置内鼓入一定量的空气。请你在下表中填写完成本实验时各装置的连接次序及药品。
| 各装置连接次序 | A | C | C | |||
| 对应的药品 | d:浓盐酸 e:固体混合物 | 碱石灰 | 碱石灰 |
(2)k@s^5*u上述高锰酸钾受热部分分解后所得固体混合物中K2MnO4与MnO2物质的量之比是 。
(3)当A装置内反应结束后,关闭分液漏斗活塞,打开止水夹k,再一次用打气筒向装置内鼓入一定量空气,其目的是 。
(4)若测得碱石灰增重ng。为了计算KMnO4的分解率α,该同学采用方法如下:设原mg的固体混合物中KMnO4及MnO2的物质的量分别为x、y,依据实验数据m及n,可列出三个含x、y、α的等式,请你写出这三个等式。(注意:等式中不用带单位)
仅含m、x、y的等式①:m= 。
仅含 n、x、y的等式②:n= 。
仅含α、x、y的等式③:α= 。
(5)另一同学设计更为简单的方法(无须化学反应)也可测定KMnO4的分解率α。
该同学的方法是:称取一定量KMnO4受热部分分解后所得的固体混合物,置于盛有适量蒸馏水的烧杯中,充分搅拌,再进行“一系列实验操作”并记录实验数据,最后经计算,即可得出KMnO4的分解率α。该同学的“一系列实验操作”是指 。
查看习题详情和答案>>