网址:http://m.1010jiajiao.com/timu_id_189100[举报]
第一组,取刚降到地面的酸雨水样,进行了如下实验:
(1)将一片红色的玫瑰花瓣浸在一份水样中
(2)每隔一定时间测定其pH,数据如表Ⅰ所示.
(3)向雨水试样中滴加氯化钡溶液,有白色浑浊出现
表Ⅰ不同时间酸雨的pH
| 测定时间/小时钟 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(2)生成白色浑浊的化学方程式
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示):
第二组,用拟用下列装置定量分析空气中SO2的含量:

(4)该组同学查资料得到的反应原理为:SO2与酸性KMnO4溶液反应的化学方程式:5SO2+2KMnO4+2H2O=2H2SO4+2MnSO4+K2SO4.
该反应的现象是
(5)KMnO4溶液中导管末端做成球状多孔结构的作用是
(6)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L.若从气体通入到紫色恰好褪去,用时5分钟.则此次取样处的空气中二氧化硫含量为
| 32bc |
| a |
| 32bc |
| a |
(10分)酸雨是指pH<5.6的雨、雪等各种形式的大气降水。二氧化硫是形成酸雨的主要因素之一,它主要是由含硫燃料(煤和石油)燃烧和金属冶炼厂释放的二氧化硫气体造成。酸雨的危害极大,减少二氧化硫等污染物的排放,保护环境是非常重要的。某校化学兴趣小组的学生,分成两组对酸雨及空气中二氧化硫的含量进行了测定。
第一组,取刚降到地面的酸雨水样,进行了如下实验:
(1)将一片红色的玫瑰花瓣浸在一份水样中
(2)向雨水试样中滴加氯化钡溶液,有白色浑浊出现
(3)每隔一定时间测定其pH,数据如表Ⅰ所示。
表Ⅰ 不同时间酸雨的pH
| 测定时间/小时钟 | 0 | 1 | 2 | 4 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 |
(1)一段时间后,观察到红色变浅,可能的原因是 ▲
(2)生成白色浑浊的离子方程式 ▲
(3)分析上述pH数据变化,你认为可能的原因是(用化学方程式表示) ▲
(4)如果取该雨水和蒸馏水混合,再测pH,结果将 ▲ (填“变大”“变小”或“不变”)
第二组,用拟用下列装置定量分析空气中SO2的含量:

(5)该组同学查资料得到的反应原理为:SO2与酸性KMnO4溶液反应的离子方程式
5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+。
该反应的现象是 ▲ ,SO2在该反应中显 ▲ (填“氧化”或“还原”)性。发生了 ▲ 反应(填“氧化”或“还原”)
(6)通入空气前应进行的实验操作是 ▲ ;KMnO4溶液中导管末端做成球状多孔结构的作用是 ▲
(7)该实验中已经知道的数据有气体流速a L/min、酸性KMnO4溶液的体积b L,其浓度为c mol/L。若从气体通入到紫色恰好褪去,用时5分钟。则此次取样处的空气中二氧化硫含量为 ▲ g/L
查看习题详情和答案>>查阅资料:Cu2O是一种碱性氧化物,溶于稀硫酸生成Cu和CuSO4.
设计探究实验:取少量粉末放入足量稀硫酸中,在所得溶液中滴加KSCN试剂.
(1)若只有Fe2O3,则实验现象是
(2)若固体粉末完全溶解无固体存在,滴加KSCN试剂时溶液不变红色,则此过程中的离子反应为:
(3)经实验分析,确定红色粉末为Cu2O和Fe2O3的混合物.实验小组欲测定Cu2O的质量分数.已知Cu2O在空气中加热生成CuO.
测定流程:

实验中操作A的名称为
灼烧过程中,所需仪器有:酒精灯、玻璃棒、
(4)写出混合物中Cu2O的质量分数的表达式
| 9(b-a) |
| a |
| 900(b-a) |
| a |
| 9(b-a) |
| a |
| 900(b-a) |
| a |
实验小组欲利用红色粉末制取较纯净的胆矾(CuSO4?5H2O).经查阅资料得知,在溶液中通过调节溶液的酸碱性而使Cu2+、Fe2+、Fe3+分别生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
实验小组设计如下实验方案制取胆矾:
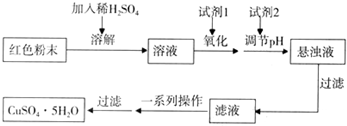
(5)用试剂编号表示:试剂l为
(6)为什么先“氧化”后“调节pH”?pH控制范围为多少?


(1)硫酸法工业流程中加入铁屑的目的是
(2)上述流程中副产品是
(3)从TiOSO4→H2TiO3需要加热,则加热的目的是
(4)用浓硫酸处理钛铁矿,并向所得溶液中加入水和铁,此时0.5L的溶液中含有2molTiO2+.4.75molSO42-.2.5mol的一种未知阳离子和H+.常温下,其溶液的pH=
(5)氯化法中熔炼过程的反应为:
2FeTiO3(s)+7Cl2(g)+6C(s)
 2TiCl4(l)+2FeCl3(s)+6CO(g)
2TiCl4(l)+2FeCl3(s)+6CO(g)该反应是在1173K的温度下进行,你认为还应该控制的反应条件是
平衡常数表达式K=
| c6(CO) |
| c7(Cl2) |
| c6(CO) |
| c7(Cl2) |
(6)熔炼后分离出四氯化钛的方法是


 2TiCl4(l)+2FeCl3(s)+6CO(g)
2TiCl4(l)+2FeCl3(s)+6CO(g)