摘要:考查运用盖斯定律进行反应热的计算:2008年高考的第29题(1)问.2007年高考的第28题的第(2)问.考查的都是应用盖斯定斯求算反应热问题.因其属于考试大纲中的新增热点.故备受高考命题的青睐.预测它在2009年的高考中将继续出现.2008年第12题.考查的是有机物的组成.结构.性质.发生的反应类型.乙烯和苯的获取过程等.主要停留在了解.识记层次.相比选修5而言.难度较低.因用它实现高考对有机化学部分的考查.有理由相信:此题目在2009年高考中仍会以选择题的形式出现.五.加大了对课本实验的考查力度.突出了中学实验基本操作.技能的考查:2008年高考化学实验很注重考查掌握化学实验的基本方法与技能.2008年第28题第问.考查的是混合物的分离与提纯,第28题的第(4)问.考查是常见离子的检验,第30题的第(2)问.考查的是一定物质的量浓度溶液的配制,第(3)问.考查氯碱工业的电解原理与过程,第(4)问.借助装置的选择考查实验室制取氢气和氯气的原理.涉及实验之多.组合之巧妙.实属罕见.可以预测.2009年的高考化学实验命题.仍是课本许多实验的巧妙组合.问题设计难度可能有所加强.考查学生实验探究能力有所加大.因此.在平时的实验教学与复习中.一定重视课本实验的复习.不要脱离了课本.同时重视实验探究能力的培养.Ⅰ部分物质分类颜 色单质名称颜色名称颜色名称颜色石墨黑色金刚石无色硅灰黑色白磷白或黄色红磷红棕色 硫淡黄色 F2淡黄绿色Cl2黄绿色Br2深红棕色I2紫黑色 铜紫红色金金色铯金色氧化物NO2红棕色N2O4无色 Na2O2淡黄色 FeO黑色Fe2O3红棕色Fe3O4黑色MnO2黑色CuO黑色Cu2O红色HgO红色Ag2O棕黑色 酸或碱碱白色碱无色 Fe(OH)2白色Fe(OH)3红褐色Cu(OH)2蓝色盐FeS黑色FeS2黄色 CuS黑色Cu2S黑色 HgS黑色PbS黑色 FeCl3?6H2O 棕褐色FeSO4?7H2O绿色 CuCl2棕黄色CuSO4白色 Cu2(OH)2CO3绿色CuSO4?5H2O 蓝色 AgCl白色AgBr淡黄色AgI黄色Ag2CO3白色Ag3PO4黄色 KMnO4紫黑色 水合离子或络离子Cu2+蓝色Fe2+浅绿色Fe3+棕黄色MnO4-紫红色[CuCl4]2- 黄色Fe(SCN) 2+ 红色颜色反应Na+黄色K+紫色注:2变成Fe(OH)3的中间产物为灰绿色.(2)CuCl2稀溶液为蓝色.浓溶液呈绿色.附表1 卤素单质及其溶液颜色卤素气态液态固态水溶液有机溶液氟淡黄绿色 氯黄绿色黄绿色 黄绿色 溴红棕色深红棕色 黄→橙色橙红→红棕色碘紫红色 紫黑色棕黄→褐色紫→紫红色注:(1)常见有机溶剂为密度小于水的苯.酒精.汽油,密度大于水的CCl4.CS2等.它们均为无色. (2)碘酒:褐色附表2 常用酸碱指示剂变色范围指示剂PH范围酸色碱色甲基橙
网址:http://m.1010jiajiao.com/timu_id_189092[举报]
已知反应①Fe(s)+CO2(g) FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;反应②CO(g)+1/2O2(g)
FeO(s)+CO(g) ΔH=a kJ·mol-1,平衡常数为K;反应②CO(g)+1/2O2(g) CO2(g) ΔH=b kJ·mol-1;反应③Fe2O3(s)+3CO(g)
CO2(g) ΔH=b kJ·mol-1;反应③Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) ΔH=c kJ·mol-1。测得在不同温度下,K值如下:
2Fe(s)+3CO2(g) ΔH=c kJ·mol-1。测得在不同温度下,K值如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)若500 ℃时进行反应①,CO2的起始浓度为2 mol·L-1,CO的平衡浓度为 。
(2)反应①为 (选填“吸热”或“放热”)反应。
(3)700 ℃时反应①达到平衡状态,要使该平衡向右移动,其他条件不变时,可以采取的措施有 (填序号)。
A.缩小反应器体积B.通入CO2C.温度升高到900 ℃D.使用合适的催化剂
E.增加Fe的量
(4)下列图像符合反应①的是 (填序号)(图中v为速率,φ为混合物中CO含量,T为温度且T1>T2)。

(5)由反应①和②可求得,反应2Fe(s)+O2(g) 2FeO(s)的ΔH= 。
2FeO(s)的ΔH= 。
(6)请运用盖斯定律写出Fe(固体)被O2(气体)氧化得到Fe2O3(固体)的热化学方程式: 。
查看习题详情和答案>>
 (1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总
(1)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同.试运用盖斯定律回答下列问题:
已知:C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g);△H1=-Q1 kJ/mol,
C2H5OH(g)=C2H5OH(l);△H2=-Q2 kJ/mol,H2O(g)=H2O(l);△H3=-Q3 kJ/mol.若使23g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
0.5Q1-0.5Q2+1.5Q3
0.5Q1-0.5Q2+1.5Q3
kJ.(2)北京奥运会祥云火炬将中国传统文化、奥运精神以及现代高科技融为一体.火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料.试回答下列问题:
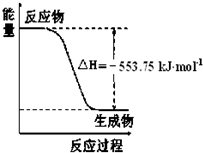
①如图是一定量丙烷完全燃烧生成CO2和1mol H2O(l)过程中的能量变化图,请写出表示丙烷燃烧热的热化学方程式
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H1=-2215.0 kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);△H1=-2215.0 kJ/mol
.②近年来已经研制出丙烷燃料电池,该电池的电解质溶液为KOH溶液,写出该电池负极的电极反应式:
C3H8-20e-+26 OH-=3CO32-+17H2O
C3H8-20e-+26 OH-=3CO32-+17H2O
.③某金属的相对原子质量为52.00,用上述电池电解该金属的一种含氧酸盐的酸性水溶液时,阳极每放出 3360ml(标准状况)氧气体,阴极析出金属 10.4g,在该含氧酸盐中金属的化合价为
+3
+3
,在该实验中,若不考虑能量的损失,电池中消耗丙烷的质量最少是1.32
1.32
g(结果精确至0.01g).?④二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔.1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量.若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
1:3
1:3
.Ⅰ.某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.已知该反应中H2O2只发生如下过程:H2O2→O2.
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)该反应中氧化剂与还原剂物质的量之比为
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
Ⅱ.已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ/mol
请运用盖斯定律写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
查看习题详情和答案>>
(1)该反应中的还原剂是
H2O2
H2O2
.(2)该反应中,发生还原反应的过程是
H2CrO4
H2CrO4
→Cr(OH)3
Cr(OH)3
.(3)该反应中氧化剂与还原剂物质的量之比为
2:3
2:3
.(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
3.36L
3.36L
.Ⅱ.已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ/mol
请运用盖斯定律写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:
CO(g)+FeO(s)=Fe(s)+CO2(g)△H=-218.0kJ/mol
CO(g)+FeO(s)=Fe(s)+CO2(g)△H=-218.0kJ/mol
. Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.
Ⅰ同素异形体相互转化的反应热相当少而且转化速率较慢,有时还很不完全,测定反应热很困难,现在可根据盖斯定律进行计算.已知:P4(s,白磷)+5O2(g)=P4O10(s)△H=-2983.2kJ?mol-1 ①
P(s,红磷)+
| 5 |
| 4 |
| 1 |
| 4 |
(1)试写出白磷转化为红磷的热化学方程式
(2)由热化学方程式来看,更稳定的磷的同素异形体是
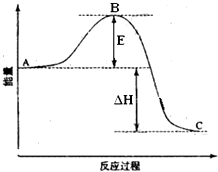
Ⅱ(6分)2SO2(g)+O2(g)═2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ?mol-1.请回答下列问题:
(1)图中E的大小对该反应的反应热有无影响?
(2)图中△H=