网址:http://m.1010jiajiao.com/timu_id_185688[举报]
一.选择题(60分)
题号
1
2
3
4
5
6
7
8
9
10
答案
B
D
A
C
C
A
C
B
D
B
题号
11
12
13
14
15
16
17
18
19
20
答案
A
C
B
D
B
B
C
D
C
B
二.填空题(34分)
21.(1) 碳碳双键 氯原子 (2) 4-甲基-3-乙基辛烷
(3) 
22、  。
。
23.(1) 4 (2)_
(CH3)
24、(1) 4 。 (2) 0 个。 (3) ⑤
25.(1) 有气泡生成(1分) , 酸性高锰酸钾溶液褪色(1分) ;
(2) 除去乙烯中的乙醇,排除干扰(2分) ;
(3)  (2分); 消去反应(1分) 。
(2分); 消去反应(1分) 。
(4) D (1分)
 26、(1) 2 5
。 (2)方程式 3 H2N―C≡N
26、(1) 2 5
。 (2)方程式 3 H2N―C≡N
 ,
,
三聚氰胺的含氮量高为66.7%(1分),可提高奶粉的含氮量,冒充蛋白质(1分)
三、计算题(6分)
27、解:(1)2.3gA中含H物质的量为: =0.3mol
(1分)
=0.3mol
(1分)
由质量守恒定律可知:m有机物 + mO2 = m(CO2) + m(CO) + m(H2O)
 ×
×
2.3gA中含C物质的量为 +
+ = 0.1mol (1分)
= 0.1mol (1分)
(2) =0.05mol (1分)
=0.05mol (1分)
该有机物中C、H、O原子个数比为:2:6:1 化学式为:C2H6O (2分)
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL溴乙烷,振荡.
实验操作Ⅱ:将试管如图固定后,水浴加热.
(1)用水浴加热而不直接用酒精灯加热的原因是
(2)观察到
(3)鉴定生成物中乙醇的结构,可用的波谱是
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是
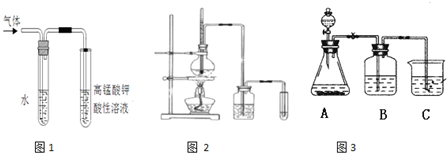
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL 溴乙烷,振荡.
实验操作II:将试管如图固定后,水浴加热.
(1)用水浴加热而不直接用酒精灯加热的原因是
(2)观察到
(3)鉴定生成物中乙醇的结构,可用的波谱是
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是
反应类型
(2)写出溴乙烷在NaOH乙醇溶液中的反应方程式
| 醇 |
| 加热 |
| 醇 |
| 加热 |
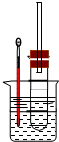
图2是实验室制乙烯并检验其性质的装置图,请回答:
(1)写出圆底烧瓶中反应的方程式
| 浓H2SO4 |
| 170℃ |
| 浓H2SO4 |
| 170℃ |
(2)烧瓶中混合液逐渐变黑,并产生某些无机杂质气体,写出产生杂质气体的化学方程式:
| ||
| ||
(3)为了检验乙烯的生成,试管中应盛放
(4)洗瓶中盛放的试剂为
某学习小组同学为了确定盐酸、苯酚、碳酸的酸性强弱,设计了如图3所示的装置图进行实验:
(1)锥形瓶内装某可溶性盐,写出A中反应的离子方程式:
(2)C中的现象为
(3)B中的试剂为
 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH水溶液和5mL 溴乙烷,振荡.
实验操作II:将试管如图固定后,水浴加热.
(1)写出该实验的反应方程式:
| ||
| △ |
| ||
| △ |
(2)用水浴加热而不直接用酒精灯加热的原因是
(3)装置中长玻璃管的作用是
(4)观察到
(5)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的物质是
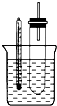 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.实验操作Ⅰ:在试管中加入5mL 1mol/L NaOH溶液和5mL溴乙烷,振荡.
实验操作Ⅱ:将试管如图固定后,水浴加热.
(1)试管口安装一长导管的作用是
(2)观察到
(3)鉴定生成物中乙醇的结构,可用的波谱是
(4)检验水解产物中的溴离子的方法是
(5)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验产物,检验的方法是