摘要:在下列空白处说明反应条件的改变对化学平衡的影响.条件的改变对化学平衡的影响增大反应物的浓度 增大容器中气体的压强 升高温度 适当使用催化剂
网址:http://m.1010jiajiao.com/timu_id_182090[举报]
1
2
3
4
5
6
7
8
9
10
C
B
B
C
B
D
A
D
B
D
11
12
13
14
15
16
17
18
19
20
B
B
B
D
A
C
A
C
B
B
21、在下列空白处说明反应条件的改变对化学平衡的影响。
条件的改变
对化学平衡的影响
增大反应物的浓度
正向移动
增大容器中气体的压强
向体积减小方向移动
升高温度
向升高温度方向移动
适当使用催化剂
不移动
22、0.3mol/(L?S)
23、加深 逆向移动 不移动
24、逐渐减小 逐渐增大 相等
25、酸性 碱性 中性
(1)已知:2SO2(g)+O2(g)?2SO3 (g)△H=-196.6kJ?mol-1;2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1 .则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=
一定条件下,将NO2与SO2 按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图1所示.该反应△H

(3)甲醇(CH3OH)燃料电池的结构示意图如图2.甲醇进入
(4)101kPa时,若16gCH3OH完全燃烧生成液态水,放出热量为363.25kJ/mol,则甲醇燃烧的热化学方程式为
查看习题详情和答案>>
-41.8
-41.8
kJ?mol-1一定条件下,将NO2与SO2 按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
b
b
.a.体系压强保持不
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图1所示.该反应△H
<
<
0(填“>”或“<”).实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失
在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失

(3)甲醇(CH3OH)燃料电池的结构示意图如图2.甲醇进入
负
负
极(填“正”或“负”),正极发生的电极反应为O2+4H++4e-═2H2O
O2+4H++4e-═2H2O
.(4)101kPa时,若16gCH3OH完全燃烧生成液态水,放出热量为363.25kJ/mol,则甲醇燃烧的热化学方程式为
CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol
CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol
.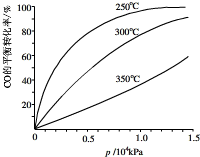 (2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
(2013?闵行区二模)研究NO2、SO2、CO等大气污染气体的处理具有重要意义.I.利用反应:6NO2+8NH3
| 催化剂 | △ |
II.一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)?SO3(g)+NO(g)-Q.
III.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)?CH3OH(g).
(1)对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2)=
0.015mol/(L?min)
0.015mol/(L?min)
.(2)对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是
bc
bc
(选填编号).a.体系压强保持不变 b.混合气体颜色保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
(3)如果Ⅱ中反应的平衡常数K值变大,该反应
a
a
(选填编号).a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(4)对于Ⅲ中的反应,CO在不同温度下的平衡转化率与压强的关系如图示.该反应是
放热
放热
反应(填“放热”或“吸热”).实际生产条件控制在250℃、1.3×104kPa左右,简述选择此压强的理由:在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
在1.3×104kPa下,CO的转化率已经很高,如果增加压强CO的转化率提高不大,而生产成本增加,得不偿失.
. (1)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1,则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=
(1)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1,则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=-41.8
-41.8
kJ?mol-1.一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是b
b
.a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1mol SO3的同时生成1molNO2
测得上述反应平衡时NO2与SO2体积比为1:6,则平衡常数K=
| 8 |
| 3 |
| 8 |
| 3 |
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如下图所示.该反应△H
<
<
0(填“>”或“<”).实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是在1.3×104Kpa下,CO转化率已较高,再增大压强CO转化率提高不大,而生产成本增加,得不偿失.
在1.3×104Kpa下,CO转化率已较高,再增大压强CO转化率提高不大,而生产成本增加,得不偿失.
. 减少NO2、SO2、CO等有害气体对大气环境的危害,是人类的共同追求.
减少NO2、SO2、CO等有害气体对大气环境的危害,是人类的共同追求.(1)在原子经济学原则引导下,化学家用CO与H2在加热加压条件合成了液体燃料甲醇,其化学反应方程式为
CO+2H2
CH3OH
| ||
| 加压 |
CO+2H2
CH3OH
.
| ||
| 加压 |
(2)以甲醇做燃料的电池,如图所示,其负极是
b
b
(填a或b),负极的反应式为
CH3OH-6e-+H2O=CO2+6H+
CH3OH-6e-+H2O=CO2+6H+
,正极的反应式为_O2+4H++4e-=2H2O
O2+4H++4e-=2H2O
.该燃料电池在理想状态下,将有96.5%的化学能转化成电能,即消耗1mol液体甲醇所能产生的最大电能达702.1kJ,则通常甲醇燃烧的热化学反应方程式为
CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-727.6kJ/mol
| 3 |
| 2 |
CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-727.6kJ/mol
.| 3 |
| 2 |
(3)已知:NO2(g)+SO2(g)?SO3(g)+NO(g)△H=+41.8kJ?mol-1 一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
b
b
.a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1mol SO3的同时生成1molNO2
当上述反应平衡时,测得NO2与SO2体积比为1:6,则平衡常数K=
| 8 |
| 3 |
| 8 |
| 3 |
当给已达平衡状态的上述反应升温时,平衡常数K′
变大
变大
.(变大、变小或不变)Ⅰ.请把符合要求的化学方程式的字母填在下列空白处:
①既属于分解反应,又属于氧化还原反应的是
②属于分解反应,但不属于氧化还原反应的是
③既属于化合反应,又属于氧化还原反应的是
④属于化合反应,但不属于氧化还原反应的是
⑤不属于四种基本反应类型的氧化还原反应的是
A.(NH4)2SO3
2NH3↑+H2O+SO2↑
B.2CO+O2
2CO2
C.2C+SiO2
Si+2CO↑
D.NH4NO3
N2O+2H2O
E.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓)
MnCl2+H2O+Cl2↑
Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为
(2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气.
①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂
查看习题详情和答案>>
①既属于分解反应,又属于氧化还原反应的是
D
D
.②属于分解反应,但不属于氧化还原反应的是
A
A
.③既属于化合反应,又属于氧化还原反应的是
B
B
.④属于化合反应,但不属于氧化还原反应的是
E
E
.⑤不属于四种基本反应类型的氧化还原反应的是
F
F
.A.(NH4)2SO3
| ||
B.2CO+O2
| ||
C.2C+SiO2
| ||
D.NH4NO3
| ||
E.CaCO3+CO2+H2O=Ca(HCO3)2
F.MnO2+4HCl(浓)
| ||
Ⅱ.(1)在一定条件下可以进行如下反应:8H2O+5R2O8n-+2Mn2+=2MnO4-+10RO42-+16H+,又知该反应中氧化剂与还原剂的物质的量之比为5:2,则R2O8n-中n的值为
2
2
.(2)反应 2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O 可用于实验室制取氯气.
①用单线桥表示出该反应的电子转移情况:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
②在标准状况下,该反应产生2.24L Cl2时,消耗氧化剂
0.04
0.04
mol,被氧化的物质的质量为7.3
7.3
g.