摘要:18.Ⅰ.用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: ①从实验装置上看.图中尚缺少的一种玻璃用品是 . ②大烧杯上如不盖硬纸板.求得的中和热数值 (填“偏大.偏小.无影响 ) ③如果用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应.与上述实验相比.所放出的热量 .所求中和热 . Ⅱ.如图所示在烧杯A.B中均盛有20℃.50mL水.试管C与D相通.其中充有红棕色气体.处于下列平衡2NO2N2O4.当向A中加入10g NaOH固体使其溶解.向B中加入50g硝酸铵也使其溶解(20℃时.硝酸铵的溶解度为197g).则: (1)A.B烧杯中.A杯溶液温度 .B杯溶液温度 (填“升高 .“降低 .“不变 ). (2)试管C中气体颜色 (填“变深 .“变浅 或“不变 ).原因是 . (3)在测定NO2的相对分子质量时.较为适宜的条件是 . .
网址:http://m.1010jiajiao.com/timu_id_1754113[举报]
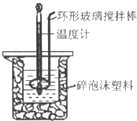 用50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液,在如图所示的装置中进行中和反应,测定强酸与强碱反应的反应热.
用50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液,在如图所示的装置中进行中和反应,测定强酸与强碱反应的反应热.
| 起始温度t1/℃ | 终止温度t2/℃ | 温度差 (t2-t1)/℃ | |||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
(2)装置中大、小烧杯之间填满碎泡沫塑料的目的是
(3)某同学实验记录的数据如上表所示,其中记录的终止温度是指
(4)计算该实验发生中和反应时放出的热量为
(5)如果用50mL 0.55mol?L一的氨水(NH3?H2O)代替NaOH溶液进行上述实验,通过测得的反应热计算中和热,其中和热△H会偏大,其原因是
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题

(1)从实验装置上看,图中尚缺少的一种玻璃用品是______________。
(2)烧杯间填满碎纸条的作用是______________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值______________(填“偏大、偏小、无影响”)
(4)实验中改用60mL 0.50mol·L-1的盐酸跟50mL 0.55mol·L-1的NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”或“不相等”),所求中和热_________ (填“相等”或“不相等”),简述理由:________________________________
查看习题详情和答案>>
(2)烧杯间填满碎纸条的作用是______________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值______________(填“偏大、偏小、无影响”)
(4)实验中改用60mL 0.50mol·L-1的盐酸跟50mL 0.55mol·L-1的NaOH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等”或“不相等”),所求中和热_________ (填“相等”或“不相等”),简述理由:________________________________
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题

(1)从实验装置上看,图中尚缺少的一种玻璃用品是________________。
(2)烧杯间填满碎纸条的作用是________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________(填“偏大、偏小、无影响”)
(4)如果用60 ml 0.50 mol/L盐酸与50mL 0.55 mol/L Na OH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等、不相等”),所求中和热___________(填“相等、不相等”), 简述理由
_____________________
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热___________的数值会 (填“偏大”、“偏小”、“无影响”)。
查看习题详情和答案>>
(2)烧杯间填满碎纸条的作用是________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值____________(填“偏大、偏小、无影响”)
(4)如果用60 ml 0.50 mol/L盐酸与50mL 0.55 mol/L Na OH溶液进行反应,与上述实验相比,所放出的热量_________(填“相等、不相等”),所求中和热___________(填“相等、不相等”), 简述理由
_____________________
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热___________的数值会 (填“偏大”、“偏小”、“无影响”)。
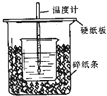 用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中尚缺少的一种玻璃用品是
环形玻璃搅拌棒
环形玻璃搅拌棒
;由图可知该装置有不妥之处,应如何改正?在大小烧杯间填满碎塑料泡沫(或碎纸条)使小烧杯口与大烧杯口相平
在大小烧杯间填满碎塑料泡沫(或碎纸条)使小烧杯口与大烧杯口相平
.(2)烧杯间填满碎塑料泡沫的作用是
保温、隔热,减少实验过程中的热最损失
保温、隔热,减少实验过程中的热最损失
.(3)如果用60mL 0.50mol/L盐酸与50mL 0.55mol/LNaOH溶液进行反应,与上述实验相比,所求得的中和热数值
相等
相等
(填“相等、不相等”)(4)用相同浓度和体积的氨水(NH3?H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会
偏小
偏小
(填“偏大”、“偏小”、“无影响”). 50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出来的热量可计算中和热.回答下列问题:
50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出来的热量可计算中和热.回答下列问题:(1)从实验装置上看,图中缺少的一种玻璃用品是
环形玻璃搅拌棒
环形玻璃搅拌棒
.(2)烧杯间填满碎纸条的作用是
防止热量损失
防止热量损失
.(3)大烧杯上如不盖硬纸板,求得的中和热数值
偏小
偏小
(填“偏大”、“偏小”或“无 影响”)(4)实验中改用60mL0.50mol/L盐酸跟50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量
不相等
不相等
,(填“相等”或“不相等”).(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
偏小
偏小
;用50mL 0.50mol/L NaOH溶液进行上述实验,测得的中和热的数值会无影响
无影响
.(均填“偏大”、“偏小”或“无影响”)