网址:http://m.1010jiajiao.com/timu_id_1754021[举报]
A.氨水 B.硫化氢气体
C.硫酸钠溶液 D.纯碱溶液
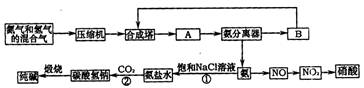
Ⅱ合成氨的流程示意图如下:

回答下列问题:
(1)工业合成氨的原料是氮气和氢气.氮气是从空气中分离出来的,通常使用的两种分离方法是
| ||
| ||
| ||
| △ |
| ||
| △ |
(2)设备A中含有电加热器、触煤和热交换器,设备A的名称
| 高温、高压 |
| 催化剂 |
| 高温、高压 |
| 催化剂 |
(3)设备B的名称
(4)设备C的作用
(5)在原料气制备过程中混有CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:
CO(g)+H2O(g)?CO2 (g)+H2 (g)
已知1000K时该反应的平衡常数K=0.627,若要使CO的转化超过90%,则起始物中c(H2O):c(CO)不低于
氨在国民经济中占有重要的地位。现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料。例如,农业上使用的氮肥如尿素、硝酸铵、磷酸铵、硫酸铵、氯化铵、氨水以及各种含氮混合肥料和复合肥料,都是以氨为原料制成的;氨氧化法制硝酸是工业上制硝酸的主要方法。
(1)下图是合成氨和利用氨制取硝酸、纯碱的简要流程示意图:

设备A的名称是 ,设备B的名称是 。
(2)硝酸厂的尾气中含有NO和NO2等污染物,为了防止污染大气可以用纯碱溶液吸收从吸收塔中放出的尾气,发生的反应如下:
Na2CO3+2NO2=NaNO2+NaNO3+CO2
但在实际生的中这种方法处理后尾气中的氮的氧化物含量仍难以降到排放标准,历此,也常利用各种燃料气中的甲烷等将氮的氧化物还原为空气主要成分而除去。写出甲烷与NO2反应的化学反应方程式: 。
(3)常压法生产出的硝酸浓度低,尾气中氮的氧化物含量高,对环境会有严重污染。可采用 法和 法进行改进。
(4)在纯碱制造过程中,过程①与过程②的顺序能否颠倒?为什么 。
查看习题详情和答案>>氨在国民经济中占有重要的地位.现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料.例如,农业上使用的氮肥如尿素、硝酸铵、磷酸铵、硫酸铵、氯化铵、氨水以及各种含氮混合肥料和复合肥料,都是以氨为原料制成的;氨氧化法制硝酸是工业上制硝酸的主要方法.
(1)下图是合成氨和利用氨制取硝酸、纯碱的简要流程示意图:
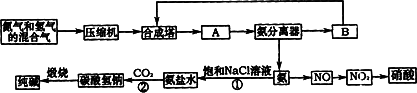
设备A的名称是________,设备B的名称是________.
(2)硝酸厂的尾气中含有NO和NO2等污染物,籽了防止污染大气可以用纯碱溶液吸收从吸收塔中放出的尾气,发生的反应如下:
Na2CO3+2NO2![]() NaNO2+NaNO3+CO2
NaNO2+NaNO3+CO2
但在实际生的中这种方法处理后尾气中的氮的氧化物含量仍难以降到排放标准,历此,也常利用各种燃料气中的甲烷等将氮的氧化物还原为空气主要成分而除去.写出甲烷与NO2反应的化学反应方程式:________.
(3)常压法生产出的硝酸浓度低,尾气中氮的氧化物含量高,对环境会有严重污染.可采用________法和________法进行改进.
(4)在纯碱制造过程中,过程①与过程②的顺序能否颠倒?为什么________.
(08枣庄三诊)氨在国民经济中占有重要的地位。现在约有80%的氨用来制造化肥,其余的用作生产其他化工产品的原料。例如,农业上使用的氮肥如尿素、硝酸铵、磷酸铵、硫酸铵、氯化铵、氨水以及各种含氮混合肥料和复合肥料,都是以氨为原料制成的;氨氧化法制硝酸是工业上制硝酸的主要方法。
|
(1)下图是合成氨和利用氨制取硝酸、纯碱的简要流程示意图:
设备A的名称是 ,设备B的名称是 。
(2)硝酸厂的尾气中含有NO和NO2等污染物,籽了防止污染大气可以用纯碱溶液吸收从吸收塔中放出的尾气,发生的反应如下:Na2CO3+2NO2====NaNO2+NaNO3+CO2
但在实际生的中这种方法处理后尾气中的氮的氧化物含量仍难以降到排放标准,历此,也常利用各种燃料气中的甲烷等将氮的氧化物还原为空气主要成分而除去。写出甲烷与NO2反应的化学反应方程式: 。
(3)常压法生产出的硝酸浓度低,尾气中氮的氧化物含量高,对环境会有严重污染。可采用 法和 法进行改进。
(4)在纯碱制造过程中,过程①与过程②的顺序能否颠倒?为什么 。
查看习题详情和答案>>
①准确称取2.3g样品,加入足量的浓硝酸充分溶解后过滤,得到滤液B.
②在B中通入过量的氨气,结果溶液呈深蓝色,同时得到1.07g红褐色沉淀.
③在②的滤液中加入足量盐酸,未见沉淀产生,再滴入足量氯化钡溶液,最后得到4.66g白色沉淀.
已知:Cu2O+2H+=Cu2++Cu+H2O,请回答下列问题:
(1)写出氨气的电子式:
(2)工业上常利用该矿物与氧气反应熔炼金属Cu,同时也得到气体C和炉渣(主要成分为Fe2O3).
①在新制的C水溶液中滴加一定量的BaCl2溶液,初始观察不到明显现象,充分振荡后,可观察到有白色沉淀产生,且逐渐增多,请解释其原因
②冶炼过程中的最后一步是氧化亚铜与硫化亚铜在高温下作用得到金属铜和气体C,写出该步骤发生反应的化学方程式
③炉渣中的氧化铁可用来制备高铁酸钾(K2FeO4).K2FeO4是一种集氧化、吸附、絮凝、杀菌、脱嗅于一体,具有绿色、环保、高效等特点的新型水处理剂.研究发现K2FeO4的氧化性比KMnO4、O3还要强,在中性、酸性溶液中稳定性较差,在碱性溶液中稳定性较好.请写出K2FeO4在强酸性溶液中释放出氧气的离子方程式