网址:http://m.1010jiajiao.com/timu_id_1754013[举报]
 根据元素周期表及周期律的知识回答下列问题:
根据元素周期表及周期律的知识回答下列问题:(1)与钠同周期且离子半径最小的元素位于周期表的第
(2)金属钠在一定条件下与氢气反应生成氢化钠(2Na+H2
| 一定条件 |
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是
a.碱性:NaOH>Mg(OH)2>Al(OH)3 b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl d.与NaOH溶液反应的剧烈程度:Na>Mg>Al
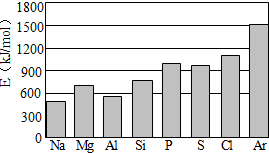
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如图所示:
①同周期内,随着原子序数的增大,E值变化的总趋势是
②根据上图提供的信息,试推断E氟
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且单质熔点最高的元素位于周期表的第_________周期第_________族。
(2)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H22NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是________。
a.离子半径:Na+>Mg2+>S2->Cl-
b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl
d. 还原性:PH3>H2S>HCl>HF
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如下图所示:
① 同周期内,随着原子序数的增大,E值变化的总趋势是__________________。
② 根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
查看习题详情和答案>>
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且单质熔点最高的元素位于周期表的第_________周期第_________族。
(2)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H2 2NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
2NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是________。
a.离子半径:Na+>Mg2+>S2->Cl-
b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl
d.还原性:PH3>H2S>HCl>HF
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如下图所示:
①同周期内,随着原子序数的增大,E值变化的总趋势是__________________。
②根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且单质熔点最高的元素位于周期表的第_________周期第_________族。
(2)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H2 2NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
2NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是________。
a.离子半径:Na+>Mg2+>S2->Cl-
b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl
d. 还原性:PH3>H2S>HCl>HF
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如下图所示:

① 同周期内,随着原子序数的增大,E值变化的总趋势是__________________。
② 根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
查看习题详情和答案>>
根据元素周期表及周期律的知识回答下列问题:
(1)与钠同周期且单质熔点最高的元素位于周期表的第_________周期第_________族。
(2)金属钠在一定条件下可与氢气反应生成氢化钠(2Na+H22NaH)。生成物氢化钠的电子式为________,含有的化学键为_____键(填“离子”、“共价”或“金属”)。
(3)元素周期表中元素的性质存在递变规律,下列比较正确的是??????________。
a.离子半径:Na+>Mg2+>S2->Cl-
b.酸性:H4SiO4>H3PO4>H2SO4>HClO4
c.氢化物稳定性:PH3<H2S<HCl
d. 还原性:PH3>H2S>HCl>HF
(4)第三周期元素的气态原子失去最外层一个电子所需能量(设为E)如下图所示:

① 同周期内,随着原子序数的增大,E值变化的总趋势是__________________。
② 根据上图提供的信息,试推断E氟_______E氧(填“>”“<”或“=”)。
查看习题详情和答案>>