摘要:15.在0.1mol/LCH3COOH溶液中存在如下电离平衡:CH3COOHCH3COO-+H+.对于该平衡.下列叙述正确的是 ( ) A.加入水.平衡向逆反应方向移动 B.加入少量NaOH固体.平衡向正反应方向移动 C.加入少量0.1mol/LHCl溶液.溶液中C(H+)减少 D.加入少量CH3COONa固体.平衡向正反应方向移动
网址:http://m.1010jiajiao.com/timu_id_1753929[举报]
常温下,将少量水加入下列物质中,相关量变化正确的是
A.AgCl悬浊液中 c(Cl-)变小 B.0.1mol/LCH3COOH溶液中 c(H+)变小
C.0.1mol/LNa2CO3 c(HCO3-)变大 D.0.1mol/LNH4Cl溶液中 n(OH-)变小
查看习题详情和答案>>
在0.1 mol/LCH3COOH溶液中存在如下电离平衡:CH3COOH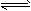 CH3COO-+H+,对于该平衡,下列叙述不正确的是
CH3COO-+H+,对于该平衡,下列叙述不正确的是
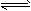 CH3COO-+H+,对于该平衡,下列叙述不正确的是
CH3COO-+H+,对于该平衡,下列叙述不正确的是[ ]
A.加入水时,平衡向正反应方向移动,溶液中n(H+)增大
B.加入少量冰醋酸,平衡向正反应方向移动,溶液中c(H+)增大
C.加入少量0.1 mol/LHCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小
D.加入少量CH3COONa同体,平衡向逆反应方向移动,溶液巾c(H+)减小
查看习题详情和答案>>
B.加入少量冰醋酸,平衡向正反应方向移动,溶液中c(H+)增大
C.加入少量0.1 mol/LHCl溶液,平衡向逆反应方向移动,溶液中c(H+)减小
D.加入少量CH3COONa同体,平衡向逆反应方向移动,溶液巾c(H+)减小
下列叙述正确的是( )
| A、无论是纯水,还是酸性,碱性或中性稀溶液,在常温时,其c(H+)?c(OH-)=1×10-14 | B、c(H+)等于1×10-7mol/L的溶液一定是中性溶液 | C、相同温度下0.2mol/LCH3COOH溶液中的c(H+)是0.1mol/LCH3COOH溶液中的c(H+)的2倍 | D、醋酸溶液稀释时,所有离子的浓度均减小 |