摘要:17.工业上冶炼铝的原料是铝土矿(主要成份为Al2O3.杂质为Fe2O3.SiO2等).某研究小组设计的提纯Al2O3的方案如下: (1)写出X.Y的化学式:X .Y , (2)通入过量CO2时反应的离子方程式为 .
网址:http://m.1010jiajiao.com/timu_id_1753707[举报]
工业上冶炼铝的原料是铝土矿(主要成份为Al2O3,杂质为Fe2O3、SiO2等).某研究小组设计的提纯Al2O3的方案如下:

(1)写出X、Y的化学式:X
(2)通入过量CO2时反应的离子方程式为
查看习题详情和答案>>

(1)写出X、Y的化学式:X
HCl
HCl
,YNaOH
NaOH
;(2)通入过量CO2时反应的离子方程式为
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
.
工业上冶炼铝的原料是铝土矿(主要成份为Al2O3,杂质为Fe2O3、SiO2等).某研究小组设计的提纯Al2O3的方案如下:

(1)写出X、Y的化学式:X ,Y ;
(2)通入过量CO2时反应的离子方程式为 . 查看习题详情和答案>>

(1)写出X、Y的化学式:X ,Y ;
(2)通入过量CO2时反应的离子方程式为 . 查看习题详情和答案>>
工业上用铝土矿(主要成份是Al2O3,还含有Fe2O3、SiO2)提取氧化铝冶炼铝的原料(纯净的Al2O3),提取操作过程如下:

请回答下列问题:
(1)请写主要成份的化学式:滤渣A
(2)反应②中Al3+反应的离子方程式为
查看习题详情和答案>>

请回答下列问题:
(1)请写主要成份的化学式:滤渣A
SiO2
SiO2
,滤液丙中的溶质是NaCl和NaHCO3
NaHCO3
.(2)反应②中Al3+反应的离子方程式为
Al3++4OH-═AlO2-+2H2O
Al3++4OH-═AlO2-+2H2O
;反应③的离子方程式为AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
AlO2-+CO2+2H2O═Al(OH)3↓+HCO3-
;反应④的化学方程式为2Al(OH)3
Al2O3+3H2O
| ||
2Al(OH)3
Al2O3+3H2O
.
| ||
工业上用铝土矿(主要成分为Al2O3,还有少量的Fe2O3,SiO2等杂质)提取氧化铝作冶炼铝的原料,提取的操作过程如下:
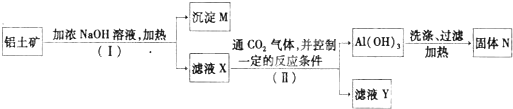
(1)Ⅰ和Ⅱ步骤中分离溶液和沉淀的操作是:
(2)沉淀M中除含有泥沙外,一定还含有
(3)滤液X中,含铝元素的溶质的化学式为
(4)实验室里常往AICl3溶液中加入
查看习题详情和答案>>

(1)Ⅰ和Ⅱ步骤中分离溶液和沉淀的操作是:
过滤
过滤
过滤
过滤
(2)沉淀M中除含有泥沙外,一定还含有
Fe2O3
Fe2O3
,固体N是Al2O3
Al2O3
;(3)滤液X中,含铝元素的溶质的化学式为
NaAlO2
NaAlO2
,它属于盐
盐
(填“酸”、“碱”或“盐”)类物质;写出Ⅰ过程所发生反应的化学方程式Al2O3+2NaOH=2NaAlO2+H2O、SiO2+2NaOH=Na2SiO3+H2O
Al2O3+2NaOH=2NaAlO2+H2O、SiO2+2NaOH=Na2SiO3+H2O
;(4)实验室里常往AICl3溶液中加入
氨水
氨水
(填“氨水”或“NaOH溶液”)来制取A1(OH)3,写出该反应的化学方程式3NH3?H2O+AlCl3=Al(OH)3+3NH4Cl
3NH3?H2O+AlCl3=Al(OH)3+3NH4Cl
.