网址:http://m.1010jiajiao.com/timu_id_1753282[举报]
 A、B、C、D、E、F六种短周期元素,原子序数依次增大,A和E同主族,A元素的原子半径最小,B元素形成的化合物目前在所有元素中种类最多,D元素原子的最外层电子数是内层电子数的3倍,A元素和F元素可形成共价化合物AF,其水溶液呈酸性.
A、B、C、D、E、F六种短周期元素,原子序数依次增大,A和E同主族,A元素的原子半径最小,B元素形成的化合物目前在所有元素中种类最多,D元素原子的最外层电子数是内层电子数的3倍,A元素和F元素可形成共价化合物AF,其水溶液呈酸性.请回答下列问题:
(1)写出下列元素的名称:C
(2)上述六种元素中,第一电离能量小的元素是
(3)A单质和D单质可形成燃料电池提供电能,请写出碱性条件下的正极电极反应式:
(4)A元素和B元素可形成自然界最简单的有机物,常温常压下,4g该有机物完全燃烧可放出222.4kJ的热量,请写出该有机物燃烧的热化学方程式:
(5)A、C、F可形成离子化合物G,G的水溶液呈弱酸性,请写出G的水溶液中各离子浓度由大到小的顺序:
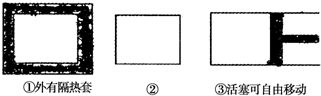
(6)如图所示,三个容积相同的容器①②③,若起始温度相同,分别向三个容器中充入3molA2和1molC2;一定条件下反应,达到平衡时各容器中CA3的百分含量由大到小的顺序为

(1)最初混合溶液中H2SO4和盐酸的物质的量浓度;
(2)当加入Ba(OH)2体积分别为20mL和40mL时,溶液的pH各为多少?(1g5=0.69,lg6=0.78)
@维生素C是一种水溶性维生素(pH<7),化学式为C6H8O6,人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸。它易被空气中的O2氧化,在新鲜的水果、蔬菜、乳制品中都富含维生素C,如新鲜橙汁中含量在500mg×L-1左右。校外活动小组测定了某牌子的橙汁中维生素C的含量,下面是实验报告单,请填写。
(1)测定目的:测定××牌橙汁维生素C的含量
(2)测定原理:C6H8O6+Ⅰ2![]() C6H6O6+2H++2I-
C6H6O6+2H++2I-
(3)实验用品及试剂:
①仪器和用品:自选(略)
②试剂:指示剂________(填名称),7.50´10-3mol×L-1标准碘溶液、蒸馏水等。
(4)实验过程:
①洗涤仪器,检查滴定管是否漏液,润洗后装好标准碘溶液待用。
②打开橙汁包装,目测:颜色——橙黄色,澄清度——好。用________(填仪器名称)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂。
③用左手控制滴定管的________(填部位),右手摇动锥形瓶,眼睛注视________直到滴定终点。滴定至终点的现象是________。
(5)数据记录与处理。(设计数据记录和数据处理的表格,不必填数据)若经数据处理,滴定中消耗标准碘溶液的体积是15.00mL,则此橙汁中维生素C的含量是________mg×L-1。
(6)问题讨论:
①滴定时能否剧烈摇动锥形瓶?为什么?答:____________________。
②从分析数据看,此软包装橙汁是不是纯天然橙汁?答:______(填编号)
|
A.是 |
B.可能是 |
C.不是 |
制造商可能采取的做法是______。
|
A.加水稀释天然橙汁 |
B.橙汁已被浓缩 |
C.将维生素C作为添加剂 |
对于上述做法,你的意见是______。
|
A.同意 |
B.不同意 |
C.调查后再作结论 |
查看习题详情和答案>>
有H2SO4和HCl的混合溶液20mL,在这个溶液中加入0.025mol×L-1的Ba(OH)2溶液,生成的BaSO4的量和相对应的溶液的pH如图所示,求解下列问题(保留两位有效数字)。

(1)最初混合溶液中H2SO4和盐酸的物质的量浓度;
(2)当加入Ba(OH)2体积分别为20mL和40mL时,溶液的pH各为多少?(1g5=0.69,lg6=0.78)
@维生素C是一种水溶性维生素(pH<7),化学式为C6H8O6,人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸。它易被空气中的O2氧化,在新鲜的水果、蔬菜、乳制品中都富含维生素C,如新鲜橙汁中含量在500mg×L-1左右。校外活动小组测定了某牌子的橙汁中维生素C的含量,下面是实验报告单,请填写。
(1)测定目的:测定××牌橙汁维生素C的含量
(2)测定原理:C6H8O6+Ⅰ2![]() C6H6O6+2H++2I-
C6H6O6+2H++2I-
(3)实验用品及试剂:
①仪器和用品:自选(略)
②试剂:指示剂________(填名称),7.50´10-3mol×L-1标准碘溶液、蒸馏水等。
(4)实验过程:
①洗涤仪器,检查滴定管是否漏液,润洗后装好标准碘溶液待用。
②打开橙汁包装,目测:颜色——橙黄色,澄清度——好。用________(填仪器名称)向锥形瓶中移入20.00mL待测橙汁,滴入2滴指示剂。
③用左手控制滴定管的________(填部位),右手摇动锥形瓶,眼睛注视________直到滴定终点。滴定至终点的现象是________。
(5)数据记录与处理。(设计数据记录和数据处理的表格,不必填数据)若经数据处理,滴定中消耗标准碘溶液的体积是15.00mL,则此橙汁中维生素C的含量是________mg×L-1。
(6)问题讨论:
①滴定时能否剧烈摇动锥形瓶?为什么?答:____________________。
②从分析数据看,此软包装橙汁是不是纯天然橙汁?答:______(填编号)
|
A.是 |
B.可能是 |
C.不是 |
制造商可能采取的做法是______。
|
A.加水稀释天然橙汁 |
B.橙汁已被浓缩 |
C.将维生素C作为添加剂 |
对于上述做法,你的意见是______。
|
A.同意 |
B.不同意 |
C.调查后再作结论 |
查看习题详情和答案>>
(一).对金属制品进行抗腐蚀处理,可延长其使用寿命。
以下为铝材表面处理的一种方法:

(1)碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出, 为将槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。 (填编号)
a.NH3 b.CO2 c.NaOH d.HNO3
(2)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,
阳极电极反应式为 。取少量废电解液,加入NaHCO3溶液,写出发生反应的离子方程式
(二).A—E五种元素中,除A、B外其他均为短周期元素它们的性质或原子结构如下表:
元素 元素性质或原子结构
A 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160
B 单质为生活中常见的金属,其相对原子质量比A大8
C 地壳中含量最多的金属元素
D 元素的主族序数是其所在周期序数的3倍
E E的某种原子的原子核内没有中子
(1)在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a KJ热量,此反应的热化学方程式是
(2)A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
(3)向2mL 0.5mol/L的ACl3溶液中加入3mL 3mol/L KF溶液,
ACl3溶液褪成无色,再加入KI溶液和CCl4振荡后静置,CCl4层不显色,
则下列说法正确的是(已知氧化性Fe3+>I2) (填字母)。
a.A3+不与I-发生反应
b.A3+与F-结合生成不与I-反应的物质
c.F-使I-的氧化性减弱
d.A3+被F-还原为A2+,使溶液中不再存在A3+
查看习题详情和答案>>
(一).对金属制品进行抗腐蚀处理,可延长其使用寿命。
以下为铝材表面处理的一种方法: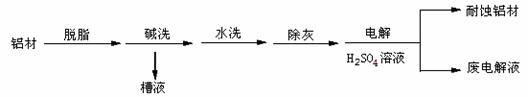
(1)碱洗的目的是除去铝材表面的自然氧化膜,碱洗时常有气泡冒出, 为将槽液中的铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。 (填编号)
a.NH3 b.CO2 c.NaOH d.HNO3
(2)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,
阳极电极反应式为 。取少量废电解液,加入NaHCO3溶液,写出发生反应的离子方程式
(二).A—E五种元素中,除A、B外其他均为短周期元素它们的性质或原子结构如下表:
| 元素 | 元素性质或原子结构 |
| A | 单质为生活中常见的金属,该金属的两种黑色氧化物(其中一种有磁性)的相对分子质量相差160 |
| B | 单质为生活中常见的金属,其相对原子质量比A大8 |
| C | 地壳中含量最多的金属元素 |
| D | 元素的主族序数是其所在周期序数的3倍 |
| E | E的某种原子的原子核内没有中子 |
(1)在高温条件下,将D、E组成的气态化合物与A的粉末充分反应,生成8gE的单质和相应的固态化合物时,放出a KJ热量,此反应的热化学方程式是
(2)A的某种氯化物溶液呈黄色,向其中通入足量SO2气体,溶液变为浅绿色,此反应的离子方程式是
(3)向2mL 0.5mol/L的ACl3溶液中加入3mL 3mol/L KF溶液,
ACl3溶液褪成无色,再加入KI溶液和CCl4振荡后静置,CCl4层不显色,
则下列说法正确的是(已知氧化性Fe3+>I2) (填字母)。
a.A3+不与I-发生反应
b.A3+与F-结合生成不与I-反应的物质
c.F-使I-的氧化性减弱
d.A3+被F-还原为A2+,使溶液中不再存在A3+ 查看习题详情和答案>>