摘要:34.[化学-物质结构与性质] 已知元素A.B.X.N.Z原子序数依次递增.Z的原子序数为29.其余的均为短周期元素.B元素的最外层电子数是其电子层数的3倍.A与N相邻.N元素原子的M电子层的P亚层中有3个未成对电子.X元素的M层电子数是其K层电子数的2倍.回答下列问题: (1)X与A可以形成一种高温结构陶瓷材料.X的氯化物分子呈正四面体结构.X的氧化物的晶体类型是______________, (2)A的具有相同化合价且可以相互转变的氧化物是_______, (3)Z2+ 的核外电子排布式是 . (4)A.N这两个元素的氢化物分子中.①氢化物的沸点从高到低排列次序是_____________.其原因是_______________ ②A.B.X.N的氢化物的化学式和立体结构分别是________________, (5)X和A所形成的结构陶瓷材料的一种合成方法如下:X的氯化物与A的氢化物加热反应.生成化合物X(AH2)4和HCl气体, X(AH2)4在高温下分解生成A的氢化物和该陶瓷材料.上述相关反应的化学方程式是 ____________________________________
网址:http://m.1010jiajiao.com/timu_id_1752584[举报]
A、B、X、Y、Z为短周期元素,它们的原子序数依次增大;A是自然界中组成化合物种类最多的元素之一:B元素的最高价氧化物对应的水化物与其简单氢化物反应生成一种盐G;元素A与Y同主族,且Y元素在短周期元素中的原子半径最大(不考虑稀有气体);Z元素的核电荷数是X的2倍.请回答下列问题:
(1)盐G的晶体内所含化学键类型是 ;在常温下测得该盐的某浓度溶液pH=6,则盐中的阴、阳离子在该溶液中的浓度之差的数值等于 (精确计算);
(2)将元素A与Z形成的化合物与过量NaOH反应生成物质F,F的水溶液在空气中长期放置发生反应,生成M和N两种物质,M与过氧化钠的结构和性质相似,则N的电子式为 ;
(3)有两种化合物同时含有上述元素中的四种相同元素,这两种化合物的水溶液混合后迅速反应,生成物中仍有一种含上述四种元素,写出该产物的化学式: ,该反应的离子方程式是 ;
(4)将由BX和BX2组成的混合气体通入下图所示的装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强(在通入混合气体之前,已通入一段时间的N2).
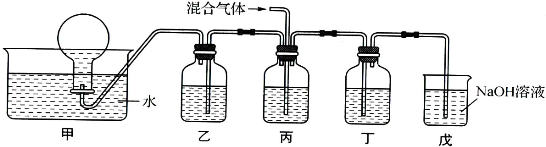
已知:①浓硝酸能将BX氧化成BX2,而稀硝酸不能氧化BX;
②NaOH溶液与BX2能发生反应生成两种盐和水,NaOH溶液与BX不反应.
a.装置乙、丙、丁中盛放的药品依次是 、 、 ;
b.能够说明实验已成功的现象是 .
查看习题详情和答案>>
(1)盐G的晶体内所含化学键类型是
(2)将元素A与Z形成的化合物与过量NaOH反应生成物质F,F的水溶液在空气中长期放置发生反应,生成M和N两种物质,M与过氧化钠的结构和性质相似,则N的电子式为
(3)有两种化合物同时含有上述元素中的四种相同元素,这两种化合物的水溶液混合后迅速反应,生成物中仍有一种含上述四种元素,写出该产物的化学式:
(4)将由BX和BX2组成的混合气体通入下图所示的装置中,用来验证浓硝酸的氧化性比稀硝酸的氧化性强(在通入混合气体之前,已通入一段时间的N2).

已知:①浓硝酸能将BX氧化成BX2,而稀硝酸不能氧化BX;
②NaOH溶液与BX2能发生反应生成两种盐和水,NaOH溶液与BX不反应.
a.装置乙、丙、丁中盛放的药品依次是
b.能够说明实验已成功的现象是
[化学-物质结构与性质]
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
(1)W基态原子的电子排步式为
(2)电负性:X
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:
(4)氨为常见化工原料,氨分子中N原子采用
已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有
A.金属键 B.离子键 C.共价键 D.配位键.
查看习题详情和答案>>
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1823 | 2751 | 11584 | 14837 |
1s22s22p63s23p63d54s1
1s22s22p63s23p63d54s1
.(2)电负性:X
>
>
Y(填“>”、“=”或“<”).(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:
氟化氢分子间形成了氢键,而氯化氢分子间只有范德华力.
氟化氢分子间形成了氢键,而氯化氢分子间只有范德华力.
.(4)氨为常见化工原料,氨分子中N原子采用
sp3
sp3
杂化,该分子的空间构型为三角锥形
三角锥形
,分子中N、H原子之间形成σ
σ
(填“σ”或“π”)键;已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有
CD
CD
.(填标号)A.金属键 B.离子键 C.共价键 D.配位键.
[化学-物质结构与性质]
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
(1)W基态原子的电子排步式为______.
(2)电负性:X______Y(填“>”、“=”或“<”).
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:______.
(4)氨为常见化工原料,氨分子中N原子采用______杂化,该分子的空间构型为______,分子中N、H原子之间形成______(填“σ”或“π”)键;
已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有______.(填标号)
A.金属键 B.离子键 C.共价键 D.配位键.
查看习题详情和答案>>
W、X、Y、Z 4种元素原子序数依次减小.W的原子序数为24;X原子p轨道共有11个电子;Y是第三周期主族元素,其部分电离能(I)如下表;Z原子价电子排布式为nsnnpn.请回答下列问题:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 | I5 |
| Y | 584 | 1823 | 2751 | 11584 | 14837 |
(2)电负性:X______Y(填“>”、“=”或“<”).
(3)R是与X同主族的短周期元素.R的氢化物沸点比X的氢化物更高,原因是:______.
(4)氨为常见化工原料,氨分子中N原子采用______杂化,该分子的空间构型为______,分子中N、H原子之间形成______(填“σ”或“π”)键;
已知W3+能与氨分子形成配离子[W(NH3)6]3+,该配离子中存在的化学键有______.(填标号)
A.金属键 B.离子键 C.共价键 D.配位键.
![]() A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D、C与F分别在同一主族,A、D两元素的原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D、C与F分别在同一主族,A、D两元素的原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
![]() (1)B元素的原子结构示意图为: ;
(1)B元素的原子结构示意图为: ;
![]() (2)由A、B、C三元素可以组成盐X,X中存在的化学键类型是: ;
(2)由A、B、C三元素可以组成盐X,X中存在的化学键类型是: ;
![]() (3)E是非金属元素,但能表现出一些金属元素的性质,请写出E与D元素的最高价氧化物的水化物反应的离子方程式: ;
(3)E是非金属元素,但能表现出一些金属元素的性质,请写出E与D元素的最高价氧化物的水化物反应的离子方程式: ;
![]() E、B两元素在一定条件下可合成用于制造轴承、永久模具的新型无机非金属材料,该材料的化学式为 ,其晶体类型是 晶体;
E、B两元素在一定条件下可合成用于制造轴承、永久模具的新型无机非金属材料,该材料的化学式为 ,其晶体类型是 晶体;
![]() (4)一定条件下,A的单质气体与B的单质气体充分反应生成6.8gW气体[已知n(A)∶n(B)=3∶1],可放出18.44kJ热量,则该反应的热化学方程式: 。
(4)一定条件下,A的单质气体与B的单质气体充分反应生成6.8gW气体[已知n(A)∶n(B)=3∶1],可放出18.44kJ热量,则该反应的热化学方程式: 。
![]() (5)F、C分别与A形成的化合物的熔、沸点A2F A2C(填“>”“<”或“=”)。
(5)F、C分别与A形成的化合物的熔、沸点A2F A2C(填“>”“<”或“=”)。
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D、C与F分别在同一主族,A、D两元素的原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)B元素的原子结构示意图为:________;
(2)由A、B、C三元素可以组成盐X,X中存在的化学键类型是:___________;
(3)E是非金属元素,但能表现出一些金属元素的性质,请写出E与D元素的最高价氧化物的水化物反应的离子方程式:_____________;E、B两元素在一定条件下可合成用于制造轴承、永久模具的新型无机非金属材料,该材料的化学式为__________,其晶体类型是________晶体;
(4)一定条件下,A的单质气体与B的单质气体充分反应生成6.8 g W气体[已知n(A)∶n(B)=3∶1],可放出18.44 kJ热量,则该反应的热化学方程式:____________。
(5)F、C分别与A形成的化合物的熔、沸点A2F________________ A2C(填“>”“<”或“=”)。
查看习题详情和答案>>
(1)B元素的原子结构示意图为:________;
(2)由A、B、C三元素可以组成盐X,X中存在的化学键类型是:___________;
(3)E是非金属元素,但能表现出一些金属元素的性质,请写出E与D元素的最高价氧化物的水化物反应的离子方程式:_____________;E、B两元素在一定条件下可合成用于制造轴承、永久模具的新型无机非金属材料,该材料的化学式为__________,其晶体类型是________晶体;
(4)一定条件下,A的单质气体与B的单质气体充分反应生成6.8 g W气体[已知n(A)∶n(B)=3∶1],可放出18.44 kJ热量,则该反应的热化学方程式:____________。
(5)F、C分别与A形成的化合物的熔、沸点A2F________________ A2C(填“>”“<”或“=”)。