摘要:14.50mL 0.1 mol·L-1的NaOH溶液被0.1 mol·L-1CH3COOH溶液中和.曲线如图所示.有关粒子浓度关系不正确的是 A.在B到D任一点.溶液中一定都有c(Na+)+c(H+)=c(CH3COO-)+c(OH-) B.在B点c(Na+)=c(CH3COO-),c(OH-)=c(H+) C.滴定过程中为定值 D.滴定过程中可能出现c(Na+)>c(CH3COO-),c(H+)>(OH-)
网址:http://m.1010jiajiao.com/timu_id_1752003[举报]
足量铜与一定量浓硝酸反应得到硝酸铜溶液和NO2、N2O4、NO 的混合气体,这些气体与0.84 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入3 mol•L-1 NaOH溶液至Cu2+ 恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.45mL B.50mL C.30mL D.60mL
查看习题详情和答案>>(1)按要求写出下列反应的离子方程式
硫酸溶液中滴加氢氧化钡溶液
(2)新制的氯水中存在Cl2、H2O、HClO、H+、Cl-、ClO-等,其中能起杀菌消毒作用的是 ;能参与Zn反应生成氢气的是 ;能与硝酸和硝酸银的混合液作用生成白色沉淀的是 ;能使染料和有机色质褪色的是 .用滴管将新制的饱和氯水缓缓滴入预先滴有酚酞试液的NaOH溶液中,当滴到一定量时红色完全褪去.产生这种现象的原因可能有两种:a是 ;b是 .
(3)①质量都是50g的HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是 ,在相同温度和相同压强条件下,体积最大的是 ,密度最小的是 .
②在 mL 0.2mol?L-1 NaOH溶液中含1g溶质;配制50mL 0.2mol?L-1 CuSO4溶液,需要CuSO4?5H2O g.
(4)在2KMnO4+16HBr═5Br2+2MnBr2+2KBr+8H2O反应中,氧化剂是 ,还原剂是 ,耗1mol氧化剂,则被氧化的还原剂的物质的量是 mol.
查看习题详情和答案>>
硫酸溶液中滴加氢氧化钡溶液
(2)新制的氯水中存在Cl2、H2O、HClO、H+、Cl-、ClO-等,其中能起杀菌消毒作用的是
(3)①质量都是50g的HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
②在
(4)在2KMnO4+16HBr═5Br2+2MnBr2+2KBr+8H2O反应中,氧化剂是
在实验室中,氮氧化物废气(主要成分NO2和NO)可以用NaOH溶液来吸收,以除去这些废气,其主要反应为:2NO2+2NaOH→NaNO2+NaNO3+H2O,NO+NO2+2NaOH→2NaNO2+H2O
(1)2molNO和2.4molNO2混合气体通入NaOH溶液被完全吸收时,生成的NaNO2 和 NaNO3物质的量各为多少?
(2)NO和NO2的混合气体的组成可表示为NOX,该混合气体通入NaOH溶液被完全吸收时,x的值可以为______(填编号).
a.1.1 b.1.2 c.1.5 d.1.8
若用纯碱溶液处理氮氧化物废气,反应与上述类似,同时放出CO2.
(3)请写出纯碱溶液吸收NO2的化学方程式______.
(4)现有标准状况下a升NO2(其中N2O4体积分数为20%)和b升NO的混合气恰好被200mL Na2CO3溶液完全吸收,则a、b应满足的关系为:______;该Na2CO3溶液的物质的量浓度为______ mol/L(用含a、b的代数式表示).
(5)若在标准状况下,2.016L氮氧化物的混合气和0.896LO2与1mol/LNa2CO3溶液50mL恰好反应生成NaNO3,则混和气体中N2O4与NO2的体积比为______.写出本小题的计算过程:______.
查看习题详情和答案>>
氨有着广泛的用途,如可用于化肥、硝酸、合成纤维等工业生产.氨的水溶液中存在电离平衡,常用电离常数Kb和电离度α来定量表示其电离程度.Kb和α常用的测定方法:在一定温度时用酸度计测定一系列已知浓度氨水的pH,可得各浓度氨水对应的c(OH-),然后通过换算求得各对应的α值和Kb值.
下面是某中学化学兴趣小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
[仪器与试剂]酸度计、50mL碱式滴定管、100mL烧杯、0.10mol?L-1 氨水
[实验数据](不必填表格)
请根据以上信息回答下述问题:
(1)25℃时,氨水的电离常数:Kb≈______,通过计算所得的数据和简洁的文字说明电离常数、电离度与弱电解质的初始浓度的关系______
(2)用0.10mol?L-1盐酸分别滴定20.00mL0.10mol?L-1的NaOH溶液和20.00mL0.10mol?L-1氨水所得的滴定曲线如下:
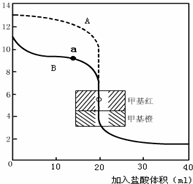
请指出盐酸滴定氨水的曲线为______(填A或B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序______.
(3)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨在燃烧试验机中相关的反应有:
4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H1①
4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H2②
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H3③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1=______.
(4)Allis-Chalmers制造公司发现可以用氨作为燃料电池的燃料.其总反应式为4NH3+3O2=2N2+6H2O,正极上的电极反应式为O2+
2H2O+4e-=4OH-,则负极上的电极反应式为______.
查看习题详情和答案>>
下面是某中学化学兴趣小组在25℃时测定一系列浓度氨水的pH所对应的c(OH-):
[仪器与试剂]酸度计、50mL碱式滴定管、100mL烧杯、0.10mol?L-1 氨水
[实验数据](不必填表格)
| 烧杯号 | V氨水 (mL) | V水(mL) | c (NH3?H2O) (mol?L-1) | c(OH-) | Kb | α |
| 1 | 50.00 | 0.00 | 1.34×10-3 | |||
| 2 | 25.00 | 25.00 | 9.48×10-4 | |||
| 3 | 5.00 | 45.00 | 4.24×10-4 |
(1)25℃时,氨水的电离常数:Kb≈______,通过计算所得的数据和简洁的文字说明电离常数、电离度与弱电解质的初始浓度的关系______
(2)用0.10mol?L-1盐酸分别滴定20.00mL0.10mol?L-1的NaOH溶液和20.00mL0.10mol?L-1氨水所得的滴定曲线如下:

请指出盐酸滴定氨水的曲线为______(填A或B),请写出曲线a点所对应的溶液中各离子浓度由大到小的排列顺序______.
(3)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨在燃烧试验机中相关的反应有:
4NH3(g)+3O2(g)=2N2(g)+6H2O(l)△H1①
4NH3(g)+5O2(g)=4NO(g)+6H2O(l)△H2②
4NH3(g)+6NO(g)=5N2(g)+6H2O(l)△H3③
请写出上述三个反应中△H1、△H2、△H3三者之间关系的表达式,△H1=______.
(4)Allis-Chalmers制造公司发现可以用氨作为燃料电池的燃料.其总反应式为4NH3+3O2=2N2+6H2O,正极上的电极反应式为O2+
2H2O+4e-=4OH-,则负极上的电极反应式为______.