网址:http://m.1010jiajiao.com/timu_id_1751871[举报]
(10分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。
(1)下列关于实验的叙述正确的有______。
| A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭 |
| B.测量溶液的pH时,应先将pH试纸润湿 |
| C.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
| D.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 |
①a g绿矾的实际质量为________ g。
②上述操作步骤的正确顺序为__________________。
③若配制时遗漏步骤④,会使所配溶液的浓度________(填“偏高”“偏低”或“无影响”)。
④若加蒸馏水时不慎超过刻度线,处理方法是________________;若操作步骤②时有溶液溅在容量瓶外,处理方法是________________。 查看习题详情和答案>>
(10分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。
(1)下列关于实验的叙述正确的有______。
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.测量溶液的pH时,应先将pH试纸润湿
C.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸
D.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
(2)要配制500 mL 0.2 mol·L-1的FeSO4溶液,实验操作步骤有:①在天平上称取a g绿矾(FeSO4·7H2O),将它放在烧杯中,用适量蒸馏水使其完全溶解;②将所得溶液沿玻璃棒注入500 mL容量瓶中;③继续向容量瓶中加水至液面距刻度线1 cm~2 cm处,改用胶头滴管加蒸馏水至液体凹液面最低处与刻度线相切;④用少量水洗涤烧杯和玻璃棒2次~3次,每次洗涤液都转入容量瓶;⑤将容量瓶塞紧,充分摇匀。填写下列空白:
①a g绿矾的实际质量为________ g。
②上述操作步骤的正确顺序为__________________。
③若配制时遗漏步骤④,会使所配溶液的浓度________(填“偏高”“偏低”或“无影响”)。
④若加蒸馏水时不慎超过刻度线,处理方法是________________;若操作步骤②时有溶液溅在容量瓶外,处理方法是________________。
查看习题详情和答案>>
(10分)化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。
(1)下列关于实验的叙述正确的有______。
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.测量溶液的pH时,应先将pH试纸润湿
C.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸
D.不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
(2)要配制500 mL 0.2 mol·L-1的FeSO4溶液,实验操作步骤有:①在天平上称取a g绿矾(FeSO4·7H2O),将它放在烧杯中,用适量蒸馏水使其完全溶解;②将所得溶液沿玻璃棒注入500 mL容量瓶中;③继续向容量瓶中加水至液面距刻度线1 cm~2 cm处,改用胶头滴管加蒸馏水至液体凹液面最低处与刻度线相切;④用少量水洗涤烧杯和玻璃棒2次~3次,每次洗涤液都转入容量瓶;⑤将容量瓶塞紧,充分摇匀。填写下列空白:
①a g绿矾的实际质量为________ g。
②上述操作步骤的正确顺序为__________________。
③若配制时遗漏步骤④,会使所配溶液的浓度________(填“偏高”“偏低”或“无影响”)。
④若加蒸馏水时不慎超过刻度线,处理方法是________________;若操作步骤②时有溶液溅在容量瓶外,处理方法是________________。
查看习题详情和答案>>
(10分,每空1分)某同学在探究废干电池内的黑色固体回收利用时,进行如图示实验:
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、三角架 、 ;
(2)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气
体,据此可初步认定黑色固体为 。
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测
滤渣中还存在的物质为 。
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1、检验Cl— | 取少许滤液于试管中,
|
| 含有Cl— |
| 2、检验NH4+ | 取少许滤液于试管中,
|
| 含有NH4+ |
| 3、检验Zn2+ | 取少许滤液于试管中,加入 稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
(5)根据以上的实验报告,关于滤液的成分,你的结论是: 。通过一定的操作从滤液中得到固体溶质, 若要将所得固体溶质中的物质加以分离,可用 法。
查看习题详情和答案>>
(10分,每空1分)某同学在探究废干电池内的黑色固体回收利用时,进行如图示实验: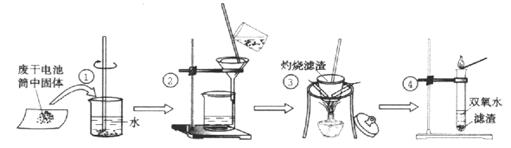
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质。请回答以下问题:
(1)操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、三角架 、 ;
(2)操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气
体,据此可初步认定黑色固体为 。
(3)操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测
滤渣中还存在的物质为 。
(4)该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2,下面是他做完实验后所写的实验报告,请你写出 其空白处的内容:
其空白处的内容:
| 实验目的 | 操作 | 实验现象 | 结论 |
| 1、检验Cl— | 取少许滤液于试管中, | | 含有Cl— |
| 2、检验NH4+ | 取少许滤液于试管中, | | 含有NH4+ |
| 3、检验Zn2+ | 取少许滤液于试管中,加入 稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |