摘要:21.已知:+1/2O2,△H =-348.3 kJ/mol +1/2O2(g) = Ag2O(s),△H =-31.0 kJ/mol 则Zn(s)+Ag2O的△H等于 ( ) A.-317.3 kJ/mol B.-379.3 kJ/mol C.-332.8 kJ/mol D.317.3 kJ/mol
网址:http://m.1010jiajiao.com/timu_id_1750679[举报]
已知:
(1) Zn(s) +l/2O2(g)=ZnO(s);△H= - 348. 3 kJ/mol
(2) 2Ag(s) +1/2O2(g)=Ag2O(s);△H= -31.0 kJ/mol
则Zn(s) +Ag2O(s)=ZnO(s) +2Ag(s)的△H等于
(1) Zn(s) +l/2O2(g)=ZnO(s);△H= - 348. 3 kJ/mol
(2) 2Ag(s) +1/2O2(g)=Ag2O(s);△H= -31.0 kJ/mol
则Zn(s) +Ag2O(s)=ZnO(s) +2Ag(s)的△H等于
[ ]
A.-317. 3 kJ/mol
B.- 379.3 kJ/mol
C.- 332. 8 kJ/mol
D.317.3 kJ/mol
查看习题详情和答案>>
B.- 379.3 kJ/mol
C.- 332. 8 kJ/mol
D.317.3 kJ/mol
 (1)经测定,20g氢气在氧气中燃烧生成水蒸气,放热2418.0kJ,写出该反应的热化学方程式
(1)经测定,20g氢气在氧气中燃烧生成水蒸气,放热2418.0kJ,写出该反应的热化学方程式2H2(g)+O2(g)=2H2O(g)△H=-483.6KJ/mol
2H2(g)+O2(g)=2H2O(g)△H=-483.6KJ/mol
;已知:3Fe (s)+2O2(g)═Fe3O4(s)△H=-1118.4kJ?mol-1,根据以上信息,则反应 3Fe(s)+4H2O(g)═Fe3O4(s)+4H2(g) 的△H=-151.2KJ/mol;
-151.2KJ/mol;
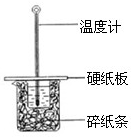
(2)某学生实验小组用50mL0.50mol?L-1的盐酸与50mL0.50mol?L-1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定
①图中装置缺少的一种仪器,该仪器名称为
环形玻璃搅拌器
环形玻璃搅拌器
.②将反应混合液的
最高
最高
温度记为反应的终止温度.③下列说法正确的是
A
A
A.小烧杯内残留有水,会使测得的反应热数值偏小
B.可用相同浓度和体积的醋酸代替稀盐酸溶液进行实验
C.烧杯间填满碎纸条的作用是固定小烧杯
D.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅.
(1)经测定,20g氢气在氧气中燃烧生成水蒸气,放热2418.0kJ,写出该反应的热化学方程式 ;已知:3Fe (s)+2O2(g)═Fe3O4(s)△H=-1118.4kJ?mol-1,根据以上信息,则反应 3Fe(s)+4H2O(g)═Fe3O4(s)+4H2(g) 的△H=
(2)某学生实验小组用50mL0.50mol?L-1的盐酸与50mL0.50mol?L-1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定
①图中装置缺少的一种仪器,该仪器名称为 .
②将反应混合液的 温度记为反应的终止温度.
③下列说法正确的是
A.小烧杯内残留有水,会使测得的反应热数值偏小
B.可用相同浓度和体积的醋酸代替稀盐酸溶液进行实验
C.烧杯间填满碎纸条的作用是固定小烧杯
D.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅.
 查看习题详情和答案>>
查看习题详情和答案>>
(2)某学生实验小组用50mL0.50mol?L-1的盐酸与50mL0.50mol?L-1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定
①图中装置缺少的一种仪器,该仪器名称为 .
②将反应混合液的 温度记为反应的终止温度.
③下列说法正确的是
A.小烧杯内残留有水,会使测得的反应热数值偏小
B.可用相同浓度和体积的醋酸代替稀盐酸溶液进行实验
C.烧杯间填满碎纸条的作用是固定小烧杯
D.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)经测定,20g氢气在氧气中燃烧生成水蒸气,放热2418.0kJ,写出该反应的热化学方程式______;已知:3Fe (s)+2O2(g)═Fe3O4(s)△H=-1118.4kJ?mol-1,根据以上信息,则反应 3Fe(s)+4H2O(g)═Fe3O4(s)+4H2(g) 的△H=______
(2)某学生实验小组用50mL0.50mol?L-1的盐酸与50mL0.50mol?L-1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定
①图中装置缺少的一种仪器,该仪器名称为______.
②将反应混合液的______温度记为反应的终止温度.
③下列说法正确的是______
A.小烧杯内残留有水,会使测得的反应热数值偏小
B.可用相同浓度和体积的醋酸代替稀盐酸溶液进行实验
C.烧杯间填满碎纸条的作用是固定小烧杯
D.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅.
查看习题详情和答案>>
(2)某学生实验小组用50mL0.50mol?L-1的盐酸与50mL0.50mol?L-1的NaOH溶液在右图所示的装置中进行中和反应反应热的测定
①图中装置缺少的一种仪器,该仪器名称为______.
②将反应混合液的______温度记为反应的终止温度.
③下列说法正确的是______
A.小烧杯内残留有水,会使测得的反应热数值偏小
B.可用相同浓度和体积的醋酸代替稀盐酸溶液进行实验
C.烧杯间填满碎纸条的作用是固定小烧杯
D.酸、碱混合时,应把量筒中的溶液缓缓倒入烧杯的溶液中,以防液体外溅.

已知化学反应①:Fe(s)+CO2(g) FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g) FeO(s)+H2(g),其平衡常数为K2。在温度973 K和
FeO(s)+H2(g),其平衡常数为K2。在温度973 K和
1173 K情况下,K1、K2的值分别如下:
| 温度 | K1 | K2 |
| 973 K | 1.47 | 2.38 |
| 1173 K | 2.15 | 1.67 |
(2)现有反应③:CO2(g)+H2(g)
 CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3= 。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3= 。(3)能判断反应③已达平衡状态的是 。
A.容器中压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(4)根据反应①与②可推导出K1、K2与K3之间的关系式 。据此关系式及上表数据,也能推断出反应③是 (填“吸热”或“放热”)反应。要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施是 (填写序号)。
A.缩小反应容器容积 B.扩大反应容器容积
C.降低温度 D.升高温度
E.使用合适的催化剂 F.设法减少CO的量 查看习题详情和答案>>