网址:http://m.1010jiajiao.com/timu_id_1749583[举报]
(1)已知 2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol;2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
①表示氢气燃烧热的热化学方程式是
| 1 |
| 2 |
| 1 |
| 2 |
②燃烧2g H2生成水蒸气,放出的热量为
(2)人们可以通过多种途径获取氢气.14g CO与适量水蒸气反应生成CO2和H2,需放出20.5kJ热量,此反应的热化学方程式为
Ⅱ.煤是化石燃料.煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后是使得到的氢气和一氧化碳在充足的空气中燃烧.这两个过程的化学方程式为:
a.C(s)+O2(g)=CO2(g)△H=E1 ①
b.C(s)+H2O(g)=CO(g)+H2(g)△H=E2 ②
H2(g)+
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
请回答:(1)上述四个热化学方程式中哪个反应△H>0?
(2)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B. a比b少 C.a与b在理论上相同
Ⅲ.已知:N2(g)+3H2(g)═2NH3(g)△H=-92.4kJ/mol
H2(g)+Cl2(g)═2HCl(g)△H=-184.6kJ/mol
| 1 |
| 2 |
| 1 |
| 2 |
计算NH3(g)+HCl(g)═NH4Cl(s)的反应焓变:△H=
(08广东实验中学三模)碳酸锰(MnCO3)是理想的高性能强磁性材料,也是制备Mn2O3、MnO2等锰的氧化物的重要原料,广泛用于电子、化工、医药等行业。一种制备MnCO3的生产流程如下图所示。
 |

软锰矿主要成分为MnO2,其中含有铁、铝、硅的氧化物和少量重金属化合物杂质,SO2来自工业废气。流程①中主要发生的反应有:MnO2 + SO2 = MnSO4 2Fe3+ + SO2 + 2H2O = 2Fe2+ + SO42― + 4H+
(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH (填“大”或“小”)该流程可与__(填工业生产名称)联合,生产效益更高。
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为 ,这样设计的目的和原理是
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀,碳酸钙的作用是 。
(4)反应④发生的化学反应为:MnSO4 + 2NH4HCO3 = MnCO3↓+ (NH4)2SO4 + CO2↑ + H2O。
反应中通常需加入稍过量的NH4HCO3 ,且控制溶液的pH为6.8~7.4。加入稍过量的NH4HCO3的目的是 ,溶液的pH不能过低的原因是 。
((5)软锰矿中锰的浸出有两种工艺:工艺A:软锰矿浆与含SO2的工业废气反应 工艺B:软锰矿与煤碳粉混合,焙烧后加稀硫酸溶解。
其中工艺A的优点是 。(答对1个即可)
查看习题详情和答案>>(1)在一定条件下,上述反应达到平衡,则混合物中碳的氧化物中碳、氧元素的质量比m(C)∶m(O)可能为__________(填选项)。
A.3∶1 B.3∶4 C.3∶5 D.3∶8
(2)设CO的转化率为75%,则碳的氧化物中m(C)∶m(O)为_________。
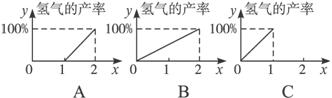
(3)现用COx表示平衡混合物中碳的氧化物的组成,则表示x与反应CO+H2O(g)![]() CO2+H2中H2产率关系正确的是________(填图象序号)。
CO2+H2中H2产率关系正确的是________(填图象序号)。