摘要:22.下表是元素周期表的一部分.针对表中的元素①一⑩.填写下列空白: (1)写出下列元素的元素符号:④ .⑩ . (2)写出⑧的离子结构示意图 . (3)表中最活泼的金属元素是 .非金属性最强的元素是 .次外层电子数是最外层电子数1/3的元素是 . (4)表中能形成两性氢氧化物的元素是 . (5)①.③两元素形成的最简单化合物的电子式为 .该化合物是由 键构成的.
网址:http://m.1010jiajiao.com/timu_id_1749042[举报]
下表是元素周期表的一部分,针对表中的①~⑧元素,填写下列空白:
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①的气态氢化物分子的空间构型为__________ ________。
(2)②的气态氢化物稳定性比⑦的气态氢化物______ ___(填“强”、“弱”或“相同”)。
(3)由①与②形成的三原子分子的电子式为_________ ___ __________。
由③与⑧形成的离子化合物的电子式为__________ ____________。
(4)③、④、⑤离子半径依次_______ ____。(填“增大”、“减小”或“不变”)
(5)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物反应离子方程式为:
。
查看习题详情和答案>>下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)元素⑩名称为
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
 .
.
(3)用电子式表示元素④与⑥的化合物的形成过程:
 ,该化合物属于
,该化合物属于
(4)写出一种由上述元素组成的既有离子键又有非极性共价键的物质的化学式
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是
查看习题详情和答案>>
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
溴
溴
在周期表中的位置第4周期第ⅦA族
第4周期第ⅦA族
.(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
HClO4
HClO4
,碱性最强的化合物的电子式是:

(3)用电子式表示元素④与⑥的化合物的形成过程:


离子
离子
(填“共价”或“离子”)化合物.(4)写出一种由上述元素组成的既有离子键又有非极性共价键的物质的化学式
Na2O2或K2O2
Na2O2或K2O2
.(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是
S2->Cl->K+
S2->Cl->K+
(用离子符号表示).下表是元素周期表的一部分,针对表中的①~⑨种元素,用适当的化学用语填写下列空白:
(1)表中最活泼的金属元素是:
(2)可用于半导体材料的元素是:
第
(3)画出元素⑦的原子结构示意图:
 ,该元素与元素⑨组成的化合物的电子式是:
,该元素与元素⑨组成的化合物的电子式是:
 .
.
(4)在第3周期元素的最高价氧化物对应水化物中,酸性最强的是:
查看习题详情和答案>>
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
K
K
.(填元素符号)(2)可用于半导体材料的元素是:
Si
Si
(填元素符号),它在元素周期表中的位置为第
3
3
周期ⅣA
ⅣA
族.(3)画出元素⑦的原子结构示意图:




(4)在第3周期元素的最高价氧化物对应水化物中,酸性最强的是:
HClO4
HClO4
(填化学式,下同);碱性最强的是:NaOH
NaOH
;具有两性的是Al(OH)3
Al(OH)3
,其与氢氧化钠溶液反应的离子方程式为:Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白.
(1)在这些元素中化学性质最不活泼的是
(2)①②⑥⑦中原子半径最小的是
(3)表中氧化性最强的单质的化学式为
(4)这些元素的最高价氧化物的水化物中,碱性最强的是
(5)⑥⑦两种元素中,离子半径较小的是
(6)④⑧⑨三种元素的气态氢化物的稳定性强弱顺序为
(7)①与③形成的化合物中,固态时俗称干冰的结构式
(8)画出⑨的原子结构示意图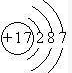
 .
.
(9)元素②的氢化物与元素⑨的氢化物反应的化学方程式为
查看习题详情和答案>>
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 | |
| 2 | ① | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | |||||
Ne
Ne
(填元素符号)(2)①②⑥⑦中原子半径最小的是
N
N
(填元素符号);(3)表中氧化性最强的单质的化学式为
F2
F2
;(4)这些元素的最高价氧化物的水化物中,碱性最强的是
NaOH
NaOH
(填化学式);(5)⑥⑦两种元素中,离子半径较小的是
Al3+
Al3+
(填离子符号);(6)④⑧⑨三种元素的气态氢化物的稳定性强弱顺序为
HF
HF
>HCl
HCl
>H2S
H2S
(填化学式);(7)①与③形成的化合物中,固态时俗称干冰的结构式
O=C=O
O=C=O
,该化合物属于共价
共价
(填“共价”或“离子”)化合物.(8)画出⑨的原子结构示意图


(9)元素②的氢化物与元素⑨的氢化物反应的化学方程式为
NH3+HCl═NH4Cl
NH3+HCl═NH4Cl
;该反应的产物属于离子
离子
(填“共价”或“离子”)化合物.下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是:
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是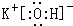
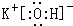 .
.
(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素④与⑥形成的化合物的形成过程: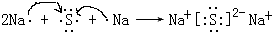
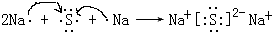 ,该化合物属于
,该化合物属于
查看习题详情和答案>>
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
Ar
Ar
(填具体元素符号,下同).(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
HClO4
HClO4
,碱性最强的化合物的电子式是: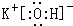
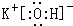
(3)最高价氧化物是两性氧化物的元素是
Al
Al
;写出它的氧化物与氢氧化钠反应的离子方程式Al2O3+2NaOH═2NaAlO2+H2O
Al2O3+2NaOH═2NaAlO2+H2O
.(4)用电子式表示元素④与⑥形成的化合物的形成过程:
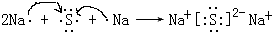
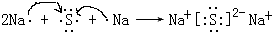
离子
离子
(填“共价”或“离子”)化合物.