摘要:15.下列物质的立体结构与CH4相同的是 A.H2O B.NH3 C.P4 D.CO2
网址:http://m.1010jiajiao.com/timu_id_1748529[举报]
 现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:
现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍.X原子的M能层上有4个未成对电子.请回答下列问题:(1)写出C、D、E三种原子第一电离能由大到小的顺序为
F>N>O
F>N>O
.(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为
H2O>NH3>CH4
H2O>NH3>CH4
,根据价层电子对互斥理论预测BA2D的分子构型为平面三角形
平面三角形
.(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-.与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上.根据其结构特点可知该晶体的化学式为(用最简正整数表示)
NaFe2(CN)6
NaFe2(CN)6
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如右图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |
TiN>MgO>KCl
TiN>MgO>KCl
.MgO晶体中一个Mg2+周围和它最邻近且等距离的O2-有6
6
个.(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是
Cr2O3
Cr2O3
.阅读以下信息,并回答问题.
数十亿年来,地球上的物质不断地变化.大气的成分也发生了很大的变化.下表是原始大气和目前空气的主要成分:
用上表所涉及的分子填写下列空白:
(1)由极性键构成的非极性分子有
(2)极易溶于水、其水溶液呈碱性的物质的分子是
(3)分子中不含孤对电子的分子(除稀有气体外)为
(4)CO的结构可表示为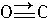 ,与CO结构最相似的分子是
,与CO结构最相似的分子是
(5)随着原始大气中O2的缓慢增加,CH4、NH3、CO等气体逐渐被氧气氧化而缓慢地减少,使大气的成分逐渐演化成目前空气.原始大气中NH3可转化为目前空气中的
(6)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合或Cu(I)(I表示化合价为+1)时,分别形成a和b:
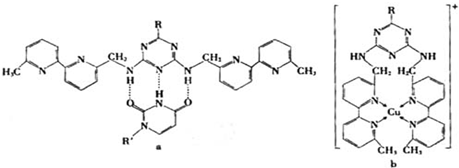
分析a和b中微粒间的相互作用(包括化学键和分子间相互作用),试指出其不同点:
a中含
查看习题详情和答案>>
数十亿年来,地球上的物质不断地变化.大气的成分也发生了很大的变化.下表是原始大气和目前空气的主要成分:
| 目前空气的主要成分 | N2、O2、CO2、水蒸气及稀有气体He、Ne等 |
| 原始大气的主要成分 | CH4、NH3、CO、CO2等 |
(1)由极性键构成的非极性分子有
CH4
CH4
和CO2
CO2
(填写化学式).(2)极易溶于水、其水溶液呈碱性的物质的分子是
NH3
NH3
(填写化学式),它之所以极易溶于水,是因为它的分子和水分子之间可形成氢
氢
键.(3)分子中不含孤对电子的分子(除稀有气体外)为
CH4
CH4
(填写化学式),它的立体构型为正四面体
正四面体
.(4)CO的结构可表示为
 ,与CO结构最相似的分子是
,与CO结构最相似的分子是N2
N2
(填写化学式),这两种结构相似的分子中,分子的极性不相同
不相同
(填“相同”或“不相同”),CO分子中有一个键的形成与另外两个不同,它叫配位
配位
键.(5)随着原始大气中O2的缓慢增加,CH4、NH3、CO等气体逐渐被氧气氧化而缓慢地减少,使大气的成分逐渐演化成目前空气.原始大气中NH3可转化为目前空气中的
N2和H2O
N2和H2O
(填化学式).(6)人工模拟是当前研究的热点.有研究表明,化合物X可用于研究模拟酶,当其结合或Cu(I)(I表示化合价为+1)时,分别形成a和b:

分析a和b中微粒间的相互作用(包括化学键和分子间相互作用),试指出其不同点:
a中含
氢键
氢键
,b中含配位键
配位键
.(用“氢键”、“配位键”、“极性键”、“非极性键”等填空)[化学--选修3:物质结构与性质]X、Y、Z、W是元素周期表中前四周期中的四种元素,其中X的原子中不存在中子,Y原于的最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.请回答下列问题: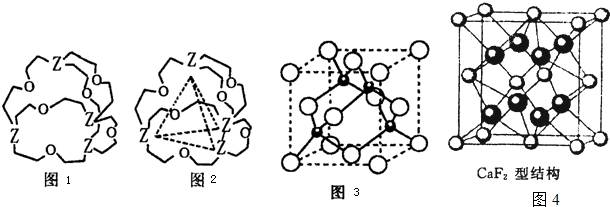
(1)写出Y原子基态时的价电子排布式: .
(2)X和Y可以形成Y2X4分子,1个Y2X4分子中含有σ键的数目为 ,其中Y原子的杂化轨道类型为 .
(3)元素Y的一种氧化物与元素2的一种氧化物互为等电子体,则元素Z的这种氧化物的分子式是 .
(4)图1表示某种含Z有机化合物的结构,其分子内4个Z原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别.下列分子或离子中,能被该有机化合物识别的是 (填标号).
A.CF4 B.CH4 C.NH
D.H2O
(5)元素W的一种氯化物晶体的晶胞结构如图3所示,该氯化物的化学式是 .已知其晶胞边长为a nm,则其晶体密度为 g?cm-3(列出算式即可).该氯化物可与浓盐酸发生非氧化还原反应,生成配合物HnWCl3,则反应的化学方程式为 .
(6)元素金(Au)与W形成的一种合金晶体具有立方最密堆积的结构,在晶胞中W原子处于面心,Au原子处于顶点位置.该晶体中原子之间的作用力是 ;该晶体具有储氢功能,氢原子可进入到由W原子与Au原子构成的四面体空隙中.若将W原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2的结构图4相似,该晶体储氢后的化学式应为 .
查看习题详情和答案>>

(1)写出Y原子基态时的价电子排布式:
(2)X和Y可以形成Y2X4分子,1个Y2X4分子中含有σ键的数目为
(3)元素Y的一种氧化物与元素2的一种氧化物互为等电子体,则元素Z的这种氧化物的分子式是
(4)图1表示某种含Z有机化合物的结构,其分子内4个Z原子分别位于正四面体的4个顶点(见图2),分子内存在空腔,能嵌入某离子或分子并形成4个氢键予以识别.下列分子或离子中,能被该有机化合物识别的是
A.CF4 B.CH4 C.NH
+ 4 |
(5)元素W的一种氯化物晶体的晶胞结构如图3所示,该氯化物的化学式是
(6)元素金(Au)与W形成的一种合金晶体具有立方最密堆积的结构,在晶胞中W原子处于面心,Au原子处于顶点位置.该晶体中原子之间的作用力是