摘要:28.铜是一种重要的金属元素.铜元素与银元素同处第ⅠB族.+1价的铜和+1价的银都可形成二配位的络离子.如..等.含铜最丰富的自然资源是黄铜矿(). (1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧.使其转变为铜.完成下列2个化学方程式: ① ② (2)但是.这种方法的缺点是副产物SO2会导致大气的污染.同时要消耗大量的热能. 现有一种湿法冶炼技术.其步骤是: ①用FeCl3.CuCl2的混合液处理富铜矿砂.使中的Cu转变为难溶的氯化物A.硫元素转变为硫单质沉淀, ②将沉淀分离出来.用氯化钠溶液处理所得的沉淀物.使A溶解变成化合物B.从而和硫单质分离, ③控制条件使B在溶液中通过歧化反应生成铜.母液中的一种成分可以在处理铜矿砂时循环使用. 回答下列问题: (1)指出A.B各是什么物质.A ,B . (2)写出①.③步中反应的化学方程式.
网址:http://m.1010jiajiao.com/timu_id_1748107[举报]
铜是一种重要的金属元素,铜元素与银元素同处第ⅠB族,+1价的铜和+1价的银都可形成二配位的络离子,如Ag(NH3)2+、AgCl2-等,含铜最丰富的天然资源是黄铜矿(CuFeS2).
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.这种方法的缺点是、.
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:
②写出反应Ⅳ中发生反应的离子方程式:
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:
④反应Ⅴ所得溶液A中含有的溶质有
查看习题详情和答案>>
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.这种方法的缺点是、.
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:
CuFeS2+3FeCl3=CuCl↓+4FeCl2+2S↓
CuFeS2+3FeCl3=CuCl↓+4FeCl2+2S↓
;②写出反应Ⅳ中发生反应的离子方程式:
Cl-+CuCl=[CuCl2]-
Cl-+CuCl=[CuCl2]-
.③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:
4FeCO3+O2═4CO2+2Fe2O3
4FeCO3+O2═4CO2+2Fe2O3
.④反应Ⅴ所得溶液A中含有的溶质有
CuCl2、NaCl
CuCl2、NaCl
.铜是一种重要的金属元素,铜元素与银元素同处第ⅠB族,+1价的铜和+1价的银都可形成二配位的络离子,如Ag(NH3)2+、AgCl2-等,含铜最丰富的天然资源是黄铜矿(CuFeS2).
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.这种方法的缺点是、.
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:______;
②写出反应Ⅳ中发生反应的离子方程式:______.
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:______.
④反应Ⅴ所得溶液A中含有的溶质有______.
查看习题详情和答案>>
铜是一种重要的金属元素,铜元素与银元素同处第ⅠB族,+1价的铜和+1价的银都可形成二配位的络离子,如Ag(NH3)2+、AgCl2-等,含铜最丰富的天然资源是黄铜矿(CuFeS2).
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.这种方法的缺点是、.
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:
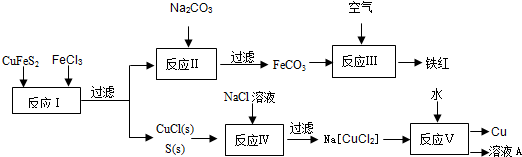
①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:______;
②写出反应Ⅳ中发生反应的离子方程式:______.
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:______.
④反应Ⅴ所得溶液A中含有的溶质有______.
查看习题详情和答案>>
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜.这种方法的缺点是、.
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高.其主要流程如下:

①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:______;
②写出反应Ⅳ中发生反应的离子方程式:______.
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:______.
④反应Ⅴ所得溶液A中含有的溶质有______.
铜是一种重要的金属元素,铜元素与银元素同处第IB族,+1价的铜和+1价的银都可形成二配位的络离子,如Ag(NH3)2+、[AgCl2]-等,含铜最丰富的天然资源是黄铜矿(CuFeS2)。
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是______________、______________。
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高。其主要流程如下
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是______________、______________。
(2)现有一种湿法冶炼技术,以黄铜矿为主要原料来生产铜、铁红颜料和可用于橡胶硫化的硫单质,原料的综合利用率较高。其主要流程如下

①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式:__________________________;
②写出反应Ⅳ中发生反应的离子方程式:____________________________。
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:____________________________。
④反应Ⅴ所得溶液A中含有的溶质有____________________________。
查看习题详情和答案>>
②写出反应Ⅳ中发生反应的离子方程式:____________________________。
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式:____________________________。
④反应Ⅴ所得溶液A中含有的溶质有____________________________。
(10分)铜是一种重要的金属元素,铜元素与银元素同处第ⅠB族,+1价的铜和+1价的银都可形成二配位的络离子,如Ag(NH3)2+、AgCl2—等,含铜最丰富的天然资源是黄铜矿(CuFeS2)。
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是 、 。
|
|
 |
①写出反应Ⅰ中FeCl3与CuFeS2所发生反应的化学方程式: ;
②写出反应Ⅳ中发生反应的离子方程式: 。
③反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式: 。
④反应Ⅴ所得溶液A中含有的溶质有 。
查看习题详情和答案>>