网址:http://m.1010jiajiao.com/timu_id_1747334[举报]
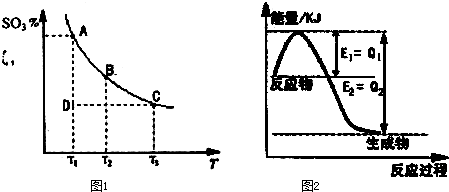
(1 )在反应:2SO2(g)+O2(g)?2SO3(g)的混合体系中,SO3的百分含量和温度的关系如图1(曲线上任何一点都表示平衡状态):
①2SO2(g)+O2(g)?2SO3(g)的△H
②当温度为T1,反应进行到状态D时,V正
(2 )①图2是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式
(△H用含Q1、Q2的代数式表示) ②25°C时,将a mol?L-1的氨水与b mol?L-1的盐酸等体积混合,所得溶液的PH=7,则c ( NH+4)
(3)海水中含有大量以化合态形式存在的氯、碘元素.
已知:25℃时,Ksp[AgCl]=1.6×10-10 mol2?L-2、Ksp[AgI]=1.5×10-16mol2?L-2).在 25℃时,向 10mL0.002mol?l-1 的 NaCl 溶液中滴入 10mL0.002mol.l-1AgNO3溶液,有白色沉淀生成,向所得浊液中继续滴入O.1mol l-1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是
运用反应原理研究氮、硫、氯、碘及其化合物的反应有重要意义。
(1)在反应:2SO2(g)+O2(g) 2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):
2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):

①2SO2(g)+O2(g) 2SO3(g)的△H
0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将
移动(填“向左”、“向右”或“不”);
2SO3(g)的△H
0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将
移动(填“向左”、“向右”或“不”);
②当温度为T1,反应进行到状态D时,V正 V逆(填“>”、“<”或“=”)。
(2)①下图是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式 。(△H用含Q1、Q2的代数式表示)

②25°C时,将a mol • L―1的氨水与b mol • L―1的盐酸等体积混合,所得溶液的pH=7,则c (NH4+) c(Cl―),a b(填“>”、“<”或“=”);
(3)海水中含有大量以化合态形式存在的氯、碘元素。已知:250C时,Ksp(AgCl)=1.6×10―10mol2•L―2、Ksp(AgI)=1.5×10―16mol2•L―2。
在 250C时,向 10mL0.002mol•L―1 的 NaCl 溶液中滴入 10mL0.002mol•L―1AgNO3溶液, 有白色沉淀生成,向所得浊液中继续滴人0.1mol •L―1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是 ,该反应的离子方程式 。
查看习题详情和答案>>
运用反应原理研究氮、硫、氯、碘及其化合物的反应有重要意义。
(1)在反应:2SO2(g)+O2(g) 2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):
2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):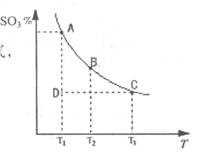
①2SO2(g)+O2(g) 2SO3(g)的△H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向左”、“向右”或“不”);
2SO3(g)的△H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向左”、“向右”或“不”);
②当温度为T1,反应进行到状态D时,V正 V逆(填“>”、“<”或“=”)。
(2)①下图是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式 。(△H用含Q1、Q2的代数式表示)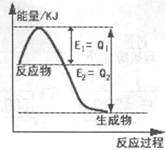
②25°C时,将a mol ? L―1的氨水与b mol ? L―1的盐酸等体积混合,所得溶液的pH=7,则c (NH4+) c(Cl―),a b(填“>”、“<”或“=”);
(3)海水中含有大量以化合态形式存在的氯、碘元素。已知:250C时,Ksp(AgCl)=1.6×10―10mol2?L―2、Ksp(AgI)=1.5×10―16mol2?L―2。
在 250C时,向 10mL0.002mol?L―1的 NaCl溶液中滴入 10mL0.002mol?L―1AgNO3溶液,有白色沉淀生成,向所得浊液中继续滴人0.1mol ?L―1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是 ,该反应的离子方程式 。
(1)在反应:2SO2(g)+O2(g)
 2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):
2SO3(g)的混合体系中,SO3的百分含量和温度的关系如下图(曲线上任何一点都表示平衡状态):
①2SO2(g)+O2(g)
 2SO3(g)的△H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向左”、“向右”或“不”);
2SO3(g)的△H 0(填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向左”、“向右”或“不”);②当温度为T1,反应进行到状态D时,V正 V逆(填“>”、“<”或“=”)。
(2)①下图是一定条件下,N2和H2发生可逆反应生成1mol NH3的能量变化图,该反应的热化学反应方程式 。(△H用含Q1、Q2的代数式表示)

②25°C时,将a mol ? L―1的氨水与b mol ? L―1的盐酸等体积混合,所得溶液的pH=7,则c (NH4+) c(Cl―),a b(填“>”、“<”或“=”);
(3)海水中含有大量以化合态形式存在的氯、碘元素。已知:250C时,Ksp(AgCl)=1.6×10―10mol2?L―2、Ksp(AgI)=1.5×10―16mol2?L―2。
在 250C时,向 10mL0.002mol?L―1的 NaCl溶液中滴入 10mL0.002mol?L―1AgNO3溶液,有白色沉淀生成,向所得浊液中继续滴人0.1mol ?L―1的NaI溶液,白色沉淀逐渐转化为黄色沉淀,其原因是 ,该反应的离子方程式 。
| 催化剂 |
| T(℃) | 0 | 50 | 100 |
| K | 0.5 | 1.05 | 2.56 |
(1)若把化学方程式写为NO+CO
| 催化剂 |
| 1 |
| 2 |
(2)上述反应达到化学平衡后,下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(3)若上述反应在容积不变的密闭容器中进行,该可逆反应达到平衡的标志是
A.气体的密度不再变化
B.单位时间内消耗的CO与生成的CO2的物质的量之比为1:1
C.气体的压强不再变化
D.各气体的浓度相等
(4)某温度下,将0.02mol的NO和0.02mol的CO的混合气体充入一装有催化剂的容器中,充分反应后,测得混合气体中CO的体积分数为0.125,则CO的转化率为