摘要:26.短周期元素X.Y.Z.W原子序数依次增大.常温时化合物XW是气体.遇氨气产生大量白烟.化合物Z2Y2是淡黄色固体. (1)请写出Y2-的电子排布式 .X可以与Y按照原子个数2:1,和1:1分别形成化合物甲和乙.化合物甲的VSEPR模型为 ,分子的立体结构为 ,键角为 ,中心原子的杂化类型为 .化合物乙的路易斯结构式为 .立体结构象翻开的书本.两个Y在书脊上.两个X分别在翻开的两个页上.据此推测是 分子.化合物乙可以看作二元弱酸.在低温.稀溶液状态下能较稳定地存在.请设计一条实验室制备少量纯净的化合乙水溶液的合成路线(用化学方程式表示出原理即可) . (2)X.Y.W三种元素共同形成的化合物中与磷酸酸性接近的是 . (3)如下图装置所示.进行下列操作: 第一步:将开关K1接通后.水槽中 附近先变红.碳棒上的电极反应式为 . 第二步:将开关K1断开.向水槽中滴入XW的溶液至红色恰好褪去.再接通开关K2.发现电流表指针偏转.写出碳棒上的电极反应式 . 第三步:一段时间后.将开关K2断开.向水槽中滴入酸性K3[Fe(CN)6]溶液.可以看到有蓝色沉淀Fe3[Fe(CN)6]2生成.标出化学式Fe3[Fe(CN)6]2中铁元素的化合价. (4)实验室常用KSCN溶液来检验Fe3+.生成配为数为n的硫氰合铁离子.写出反应的离子方程式 .Z2Y2可与氯化亚铁溶液反应产生红褐色沉淀和能使带火星木条复燃的气体.若沉淀和气体的物质的量之比为2:1.反应的化学方程式是 . (5)等体积.等物质的量浓度的下列四种配合物的水溶液.配离子的电荷数最高的是 .分别向其中加入过量的AgNO3溶液.不能生成沉淀的是 ,将生成的沉淀过滤.洗涤.干燥.称量.得沉淀a克.再向滤液中加入适量的稀硝酸后.又有沉淀生成的是 ,同样将生成的沉淀过滤.洗涤.干燥.称量.得沉淀b克.如果b=2a.则应是 . ①[Co(NH3)4 Cl2]Cl ②[Co(NH3)3 Cl3] ③[Co(NH3)6]Cl3 ④[Co(NH3)5 Cl]Cl2
网址:http://m.1010jiajiao.com/timu_id_1747216[举报]
短周期元素X、Y、Z、W的原子序数依次增大,X的原子在元素周期表中原子半径最小,Y原子基态时最外层电
子数是次外层的3倍,ZX2中Z是一种储氢材料,W与Y属于同一主族.下列叙述正确的是( )
子数是次外层的3倍,ZX2中Z是一种储氢材料,W与Y属于同一主族.下列叙述正确的是( )
| A、原子半径:rW>rZ>rY | B、元素Y的简单气态氢化物的热稳定性比W的弱 | C、化合物从X2Y、ZY、WY3中化学键的类型相同 | D、化合物ZWY4?7X2Y的水溶液显酸性 |
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族.
(1)W元素在周期表中的位置为
(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于
(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g C气体(已知n(X):n(Y)=3:1)可放出18.44kJ热量,则该反应的热化学方程式为
(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol D能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下D与NaOH溶液反应的离子方程式
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式
(5 )X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为
查看习题详情和答案>>
(1)W元素在周期表中的位置为
第三周期第VⅠA族
第三周期第VⅠA族
;写出Y元素原子的价电子排布式:2S22P3
2S22P3
;(2)由X、Z两元素可以组成A、B两种化合物,A在一定条件下可以分解成B,A的分子属于
极性
极性
(填“极性”、“非极性”)分子.(3)一定条件下,Y的单质气体与X的单质气体充分反应生成6.8g C气体(已知n(X):n(Y)=3:1)可放出18.44kJ热量,则该反应的热化学方程式为
N2(g)+3H2(g) 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol
 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/molN2(g)+3H2(g) 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol
. 2NH3(g)△H=-92.2kJ/mol
2NH3(g)△H=-92.2kJ/mol(4)由X、Y、Z、W四种元素组成的一种离子化合物D
①已知1mol D能与足量NaOH浓溶液反应生成标准状况下44.8L气体.写出加热条件下D与NaOH溶液反应的离子方程式
NH4++OH-
H2O+NH3↑
| ||
NH4++OH-
H2O+NH3↑
.
| ||
②又知D既能与盐酸反应,又能与氯水反应,写出D与氯水反应的离子方程式
SO32-+Cl2+H2O═SO42-+2Cl-+2H+
SO32-+Cl2+H2O═SO42-+2Cl-+2H+
.(5 )X的单质与Z的单质在KOH的浓溶液中可以形成原电池,如果以金属M和金属N为惰性电极,在电池的M极通入X的单质气体,N极通入Z的单质气体,则M极的电极反应式为
H2+2OH--2e-═2H2O
H2+2OH--2e-═2H2O
.短周期元素X、Y、Z、W原子序数依次增大.X氢化物的水溶液显碱性;Y在元素周期表中所处的周期序数与族序数相等;Z单质是将太阳能转化为电能的常用材料;W是重要的“成盐元素”,主要以钠盐的形式存在于海水中.请回答:
(1)Y在元素周期表中的位置是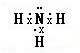
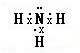 .
.
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈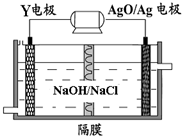
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如图所示.该电池的负极反应式是
(4)Z和W比较,非金属性较弱的是
a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H-Z或H-W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性.
查看习题详情和答案>>
(1)Y在元素周期表中的位置是
第三周期第ⅢA族
第三周期第ⅢA族
;X氢化物的电子式是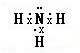
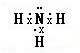
(2)X氢化物的水溶液与W氢化物的水溶液混合后恰好反应时,溶液呈
酸
酸
(填“酸”、“碱”或“中”)性,用离子方程式表示其原因是NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
.
(3)Y-AgO电池是应用广泛的鱼雷电池,其原理如图所示.该电池的负极反应式是
Al+4OH--3e-=AlO2-+2H2O
Al+4OH--3e-=AlO2-+2H2O
.(4)Z和W比较,非金属性较弱的是
Si
Si
(填元素符号),下列可以验证这一结论的是bcd
bcd
(填序号).a.元素在地壳中的含量
b.最高价氧化物对应水化物的酸性
c.断开氢化物中1mol H-Z或H-W键所需的能量
d.Z与W以共价键形成化合物时,Z或W显示的电性.
 有原子序数依次增大的4种短周期元素X、Y、Z、W,已知:
有原子序数依次增大的4种短周期元素X、Y、Z、W,已知:①X与Z、Y与W分别同主族;
②X、Z、W分别与Y都能形成两种常见的化合物;
③Y的阴离子与Z的阳离子核外电子排布相同,试根据以上叙述填空:
(1)写出由Y与Z形成的化合物Z2Y2的电子式:


H2O2+SO2=H2SO4
H2O2+SO2=H2SO4
(2)用离子方程式表示只含X、Z、W三种元素的化合物的水溶液呈碱性的原因:
亚硫酸氢钠是强碱弱酸酸式盐,亚硫酸氢根离子水解而使其溶液呈碱性
亚硫酸氢钠是强碱弱酸酸式盐,亚硫酸氢根离子水解而使其溶液呈碱性
(3)有两种化合物都只含上述四种元素,它们在水溶液中发生反应生成气体的离子方程式为:
H++HSO3-=H2O+SO2↑
H++HSO3-=H2O+SO2↑
(4)X、Y两种元素的单质已经被应用于飞船的燃料电池中,如图所示,两个电极都由多孔性碳构成,通入的两种单质由空隙逸出并在电极表面放电.①a是装置的
负
负
极.②b极上的电极反应式是O2+4e-+2H2O=4OH-
O2+4e-+2H2O=4OH-
. 短周期元素X、Y、Z、W在元素周期表中的位置如下图所示,若W原子最外层电子数是其内层电子总数的
短周期元素X、Y、Z、W在元素周期表中的位置如下图所示,若W原子最外层电子数是其内层电子总数的