网址:http://m.1010jiajiao.com/timu_id_1746730[举报]
(1)产生上述实验现象的试剂组合有(请用字母代号逐一列出,表格各栏可填满,可不填满,也可补充)
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 甲 | B | |||||||
| 乙 | D |
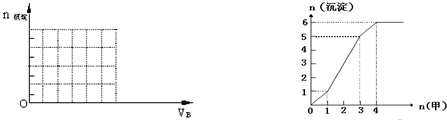
(3)如图是某一组实验中所得沉淀的物质的量(n沉淀/mol)随甲溶液中溶质的物质的量(n甲/mol)变化的曲线.符合图(右)曲线的试剂组合是:甲
A组:①苯酚,②冰醋酸,③油脂,④溴乙烷;
B组:⑤溴水,⑥甲醛,⑦氢氧化钠溶液,⑧氯化铁溶液.
A组物质中有一种跟B组物质均能反应,B组物质中有一种跟A组物质均能反应,则这两种物质分别是( )
| A、①⑦ | B、③⑧ | C、①⑥ | D、②⑦ |
(1)写出电解饱和氯化钠溶液时的电极反应式和总的离子反应方程式。?
阳极: ,阴极: ;?
总反应方程式: 。?
(2)离子交换膜电解槽一般采用金属钛作阳极,其原因是 ,阴极一般用碳钢网制成。阳离子交换膜把电解槽隔成阴极室和阳极室,其作用是 。
(3)为使电解氯化钠的速率加快,下列措施可行的是 。
a.增大阴极碳钢网面积 b.提高饱和氯化钠溶液的温度
c.加大阴极与阳极间的距离 d.提高电解时的电源电压?
(4)电解之前食盐水需要精制,目的是除去粗盐中的Ca2+、Mg2+、SO2-4等杂质离子,使用的试剂有:?a.Na2CO3?溶液; b.Ba(OH)2溶液; c.稀盐酸。其合理的加入顺序为 (填试剂序号)。
(5)如果在容积为10 L的离子交换膜电解槽中,1 min在阴极可产生11.2 L(标准状况)Cl2,这时溶液的pH是(设体积维持不变) 。?
(6)Cl2常用于自来水的消毒杀菌,现在有一种新型消毒剂ClO2,若它们在杀菌过程中的还原产物均为Cl-,消毒等量的自来水,所需用Cl2和ClO2的物质的量之比为 。?
查看习题详情和答案>>有下列七种溶液:A、氢氧化钠溶液;B、氢氧化钡溶液;C、硫酸铝溶液;D、明矾溶液;E、混有少量硝酸的硫酸镁溶液;F、氯化铁溶液;任取其中的一种溶液(甲)逐滴加入到另一种溶液(乙)中至过量,观察到自始至终均有白色沉淀。试回答下列问题:
(1)产生上述实验现象的试剂组合有(请用字母代号逐一列出,表格各栏可填满,可不填满,也可补充)
|
组别 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
甲 |
B |
|
|
|
|
|
|
|
|
乙 |
D |
|
|
|
|
|
|
|
(2)请在下列坐标中作出第1组实验所得沉淀的物质的量(n沉淀/mol)随B溶液体积(VB/L)变化的曲线。

(3)下图是某一组实验中所得沉淀的物质的量(n沉淀/mol)随甲溶液中溶质的物质的量(n甲/mol)变化的曲线。符合下图曲线的试剂组合是:甲 (填化学式);乙 (填化学式)。

若实验时取用的乙溶液为500 mL,试计算乙溶液中溶质的物质的量的浓度
查看习题详情和答案>>
(1)产生上述实验现象的试剂组合有(请用字母代号逐一列出,表格各栏可填满,可不填满,也可补充)
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 甲 | B | |||||||
| 乙 | D |
(3)如图是某一组实验中所得沉淀的物质的量(n沉淀/mol)随甲溶液中溶质的物质的量(n甲/mol)变化的曲线.符合图(右)曲线的试剂组合是:甲______(填化学式)、乙______(填化学式).
