网址:http://m.1010jiajiao.com/timu_id_1745886[举报]
磁材氧化铁的化学名称是氧化铁(Fe2O3),它是电子、电信工业的磁性材料,工业上采用生产钛白粉的下脚料(含大量FeSO4溶液)制备磁材氧化铁的步骤如下:
①向下脚料(含大量FeSO4溶液)中加入少量2 mo1·L-1叫H2SO4和铁皮;
②向①中所得溶液中加絮凝剂和水,经过滤除去吸附了杂质的絮凝剂;
③将②所得的滤液浓缩结晶得到晶体A;
④将晶体A溶于水,并加入NH4HCO3,产生CO2气体同时得到FeCO3沉淀和无色溶液C;
⑤将FeCO3沉淀洗涤、烘干并煅烧。(煅烧中的变化为:FeCO3=FeO+CO2↑; 4FeO+O2=2 Fe2O3)
据上述信息回答下列问题:
(1)用18.4mo1·L-1的H2SO4配制500mL 2 mo1·L-1H2SO4,所需玻璃仪器除
mL量筒、玻璃棒、烧杯、500mI。容量瓶外,还需要 。
(2)步骤①中2 mo1·L-1H2SO4和铁皮的作用分别为 。
(3)晶体A的化学式为 ,检验溶液C中溶质阳离子的方法是 。
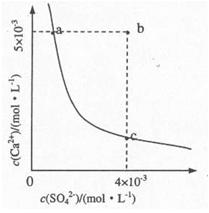
(4)向溶液C中加入CaCl2溶液能得到CaSO4沉淀,常温下KSP(CaSO4)=9x10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。
①a点对应的KSP c点对应的KSP填“大于”、“小于”或“等于”);
②若由b点变到a点下列措施可行的是 。
A.加入适量CaCl2 B.加入适量BaCl2.
C.加人适量Na2SO4 D.蒸发
查看习题详情和答案>>磁材氧化铁的化学名称是氧化铁(Fe2O3),它是电子、电信工业的磁性材料,工业上采用生产钛白粉的下脚料(含大量FeSO4溶液)制备磁材氧化铁的步骤如下:
①向下脚料(含大量FeSO4溶液)中加入少量2 mo1·L-1叫H2SO4和铁皮;
②向①中所得溶液中加絮凝剂和水,经过滤除去吸附了杂质的絮凝剂;
③将②所得的滤液浓缩结晶得到晶体A;
④将晶体A溶于水,并加入NH4HCO3,产生CO2气体同时得到FeCO3沉淀和无色溶液C;
⑤将FeCO3沉淀洗涤、烘干并煅烧。(煅烧中的变化为:FeCO3=FeO+CO2↑; 4FeO+O2=2 Fe2O3)
据上述信息回答下列问题:
(1)用18.4mo1·L-1的H2SO4配制500mL 2 mo1·L-1H2SO4,所需玻璃仪器除
mL量筒、玻璃棒、烧杯、500mI。容量瓶外,还需要 。
(2)步骤①中2mo1·L-1H2SO4和铁皮的作用分别为 。
(3)晶体A的化学式为 ,检验溶液C中溶质阳离子的方法是 。
(4)向溶液C中加入CaCl2溶液能得到CaSO4沉淀,常温下KSP(CaSO4)=9x10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。
①a点对应的KSP c点对应的KSP填“大于”、“小于”或“等于”);
②若由b点变到a点下列措施可行的是 。
A.加入适量CaCl2 B.加入适量BaCl2.
C.加人适量Na2SO4 D.蒸发
查看习题详情和答案>>
(16分)磁材氧化铁的化学名称是氧化铁(Fe2O3),它是电子、电信工业的磁性材料,工业上采用生产钛白粉的下脚料(含大量FeSO4的废液)为原料来制备磁材氧化铁。
已知煅烧中的化学反应方程式为:FeCO3 → FeO + CO2↑,4FeO + O2 → 2Fe2O3
(1)用98%的H2SO4的配制500mL的20%的H2SO4,所需玻璃仪器是
A、玻璃棒 B、烧杯 C、漏斗 D、250mL容量瓶
E、500mL容量瓶 F、胶头滴管
(2)浓缩结晶后得到的晶体是 (填化学式),A中溶质是 ;
此溶液中各离子的浓度比较大小为: 。
(3)20%H2SO4和铁皮的作用分别是 。
(4)检验滤液中含有NH4+的方法是
(5)写出步骤“合成”中发生的化学变化(用化学方程式表示):
。
查看习题详情和答案>>
磁材氧化铁的化学名称是氧化铁(Fe2O3),它是电子、电信工业的磁性材料,工业上采用生产钛白粉的下脚料(含大量FeSO4溶液)制备磁材氧化铁的步骤如下:
①向下脚料(含大量FeSO4溶液)中加入少量2 mo1·L-1叫H2SO4和铁皮;
②向①中所得溶液中加絮凝剂和水,经过滤除去吸附了杂质的絮凝剂;
③将②所得的滤液浓缩结晶得到晶体A;
④将晶体A溶于水,并加入NH4HCO3,产生CO2气体同时得到FeCO3沉淀和无色溶液C;
⑤将FeCO3沉淀洗涤、烘干并煅烧。(煅烧中的变化为:FeCO3="FeO+CO2↑; " 4FeO+O2="2" Fe2O3)
据上述信息回答下列问题:
(1)用18.4mo1·L-1的H2SO4配制500mL 2 mo1·L-1H2SO4,所需玻璃仪器除
mL量筒、玻璃棒、烧杯、500mI。容量瓶外,还需要 。
(2)步骤①中2 mo1·L-1H2SO4和铁皮的作用分别为 。
(3)晶体A的化学式为 ,检验溶液C中溶质阳离子的方法是 。
(4)向溶液C中加入CaCl2溶液能得到CaSO4沉淀,常温下KSP(CaSO4)=9x10-6,常温下CaSO4在水中的沉淀溶解平衡曲线如图所示。
①a点对应的KSP c点对应的KSP填“大于”、“小于”或“等于”);
②若由b点变到a点下列措施可行的是 。
| A.加入适量CaCl2 | B.加入适量BaCl2. |
| C.加人适量Na2SO4 | D.蒸发 |
(16分)磁材氧化铁的化学名称是氧化铁(Fe2O3),它是电子、电信工业的磁性材料,工业上采用生产钛白粉的下脚料(含大量FeSO4的废液)为原料来制备磁材氧化铁。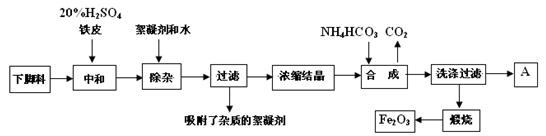

已知煅烧中的化学反应方程式为:FeCO3 → FeO + CO2↑,4FeO + O2 → 2Fe2O3
(1)用98%的H2SO4的配制500mL的20%的H2SO4,所需玻璃仪器是
| A.玻璃棒 | B.烧杯 | C.漏斗 | D.250mL容量瓶 |
(2)浓缩结晶后得到的晶体是 (填化学式),A中溶质是 ;
此溶液中各离子的浓度比较大小为: 。
(3)20%H2SO4和铁皮的作用分别是 。
(4)检验滤液中含有NH4+的方法是
(5)写出步骤“合成”中发生的化学变化(用化学方程式表示):
。 查看习题详情和答案>>