摘要:26. I.A.B.C.D是元素周期表中短周期元素.原子序数依次增大. 元素 结构或性质 A 原子最外层电子数和电子层数相等 B B和A形成的化合物甲.空间构型三角锥形 C 与地壳中含量最多的元素同主族 D 单质为有色气体 (1)甲的电子式是 . (2)C的非金属性比D的非金属性 .并用化学事实加以说明 . 20090414 (3)B2A4是一种高能燃料.已知0.5mol液态B2A4在空气中燃烧时生成气体B2和液态水时放出314.5 kJ热量.该反应的热化学方程式是 . II.合成氨生产技术的创立开辟了人工固氮的途径.对化学工业技术也产生了重大影响.合成氨反应的化学方程式为: . .合成氨工业中原料气N2可从空气中分离得到.H2可用甲烷在高温下与水蒸气反应制得.我国合成氨工业目前的生产条件为:催化剂一铁触媒.温度一400-500℃.压强一30-50MPa. 回答下列问题: (1)合成氨工业中原料气压缩到30-50MPa的原因是 .从平衡移动原理分析.低温有利于原料气的转化.实际生产中采用400-500℃的高温.原因之一是考虑到 .原因之二是增加反应速率.缩短达到平衡的时间. (2)500℃.50MPa时.在容积为VL的容器中加入 mol N2.3 mol H2.反应达平衡后测得平衡常数为K.此时N2的转化率为 .则K和的关系满足K= . (3)有人设想寻求合适的催化剂和电极材料.以N2.H2为电极反应物.以HCl一NH4CI为电解质溶液制取新型燃料电池.请写出该电池的正极反应式 .
网址:http://m.1010jiajiao.com/timu_id_1745713[举报]
A、B、C、D、E为中学化学常见的单质或化合物,其相互转化关系如图甲所示.

(1)若A为短周期常见金属单质,B、C均为含A元素的盐,且B溶液的pH>7,C溶液pH<7.用离子方程式表示B溶液pH>7的原因
(2)若A是淡黄色化合物;常温下D是无色气体;C为常见强碱,含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是
②写出反应I的化学方程式
③将一定量的气体D通入2L C的溶液中,向所得溶液中边逐滴加入稀盐酸 边振荡至过量,产生的气体与盐酸物质的量的关系如图乙(忽略气体的溶解和HCl的挥发).请回答:O点溶液中所含溶质的化学式为
查看习题详情和答案>>

(1)若A为短周期常见金属单质,B、C均为含A元素的盐,且B溶液的pH>7,C溶液pH<7.用离子方程式表示B溶液pH>7的原因
AlO2-+2H2O=Al(OH)3+OH-
AlO2-+2H2O=Al(OH)3+OH-
;(2)若A是淡黄色化合物;常温下D是无色气体;C为常见强碱,含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是
离子键和共价键
离子键和共价键
;②写出反应I的化学方程式
2Na2O2+2CO2═2Na2CO3+O2
2Na2O2+2CO2═2Na2CO3+O2
;③将一定量的气体D通入2L C的溶液中,向所得溶液中边逐滴加入稀盐酸 边振荡至过量,产生的气体与盐酸物质的量的关系如图乙(忽略气体的溶解和HCl的挥发).请回答:O点溶液中所含溶质的化学式为
NaOH和Na2CO3
NaOH和Na2CO3
,a点溶液中各离子浓度由大到小的顺序是Na+>Cl->HCO3->OH->H+>CO32-
Na+>Cl->HCO3->OH->H+>CO32-
.A、B、C、D、E为中学化学常见的单质或化合物,其相互转化关系如图甲所示.
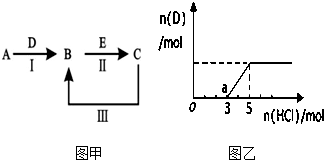
(1)若A为短周期常见金属单质,B、C均为含A元素的盐,且B溶液的pH>7,C溶液pH<7.用离子方程式表示B溶液pH>7的原因______;
(2)若A是淡黄色化合物;常温下D是无色气体;C为常见强碱,含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是______;
②写出反应I的化学方程式______;
③将一定量的气体D通入2L C的溶液中,向所得溶液中边逐滴加入稀盐酸 边振荡至过量,产生的气体与盐酸物质的量的关系如图乙(忽略气体的溶解和HCl的挥发).请回答:O点溶液中所含溶质的化学式为______,a点溶液中各离子浓度由大到小的顺序是______.
查看习题详情和答案>>
A、B、C、D、E为中学化学常见的单质或化合物,其相互转化关系如图甲所示.
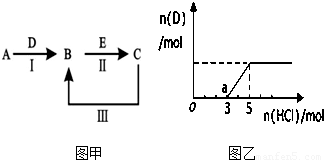
(1)若A为短周期常见金属单质,B、C均为含A元素的盐,且B溶液的pH>7,C溶液pH<7.用离子方程式表示B溶液pH>7的原因______;
(2)若A是淡黄色化合物;常温下D是无色气体;C为常见强碱,含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是______;
②写出反应I的化学方程式______;
③将一定量的气体D通入2L C的溶液中,向所得溶液中边逐滴加入稀盐酸 边振荡至过量,产生的气体与盐酸物质的量的关系如图乙(忽略气体的溶解和HCl的挥发).请回答:O点溶液中所含溶质的化学式为______,a点溶液中各离子浓度由大到小的顺序是______.
查看习题详情和答案>>

(1)若A为短周期常见金属单质,B、C均为含A元素的盐,且B溶液的pH>7,C溶液pH<7.用离子方程式表示B溶液pH>7的原因______;
(2)若A是淡黄色化合物;常温下D是无色气体;C为常见强碱,含有的阴、阳离子均为10电子粒子.
①C中所含化学键的类型是______;
②写出反应I的化学方程式______;
③将一定量的气体D通入2L C的溶液中,向所得溶液中边逐滴加入稀盐酸 边振荡至过量,产生的气体与盐酸物质的量的关系如图乙(忽略气体的溶解和HCl的挥发).请回答:O点溶液中所含溶质的化学式为______,a点溶液中各离子浓度由大到小的顺序是______.
查看习题详情和答案>>
A、B、C、D、E、F、G、L、I九种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E、B与G、D与L分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F的2倍,C和D的最外层电子数之和为11.请回答下列问题:
(1)以上八种元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)________,E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)________>________>________.
(2)由L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为________.固体化合物E2D2投入到化合物E2 L的水溶液中,只观察到有沉淀产生的,写出该反应的离子方程式为:________.
(3)在10 L的密闭容器中,通入2 mol LD2气体和1 mol D2气体,一定温度下反应后生成LD3气体,当反应达到平衡时,D2的浓度为0.01 mol·L-1,同时放出约177 kJ的热量,则平衡时LD2的转化率为________;该反应的热化学方程式为________;此时该反应的平衡常数K=________.
(4)有人设想寻求合适的催化剂和电极材料,以C2、A2为电极反应物,以HCl一NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式________;放电时溶液中H+移向________(填“正”或“负”)极.
 Ⅰ、有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的
Ⅰ、有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的| 3 |
| 4 |
(1)写出相应元素符号,A
H
H
BN
N
CO
O
ES
S
(2)X溶液呈酸性,其原因是
NH4++H2O NH3?H2O+H+
NH3?H2O+H+
 NH3?H2O+H+
NH3?H2O+H+NH4++H2O NH3?H2O+H+
NH3?H2O+H+
(用离子方程式表示). NH3?H2O+H+
NH3?H2O+H+(3)由A、C、D、E四种元素所组成的一种中学常见的化合物,它既能与盐酸反应,又能与NaOH溶液反应,在这种化合物的水溶液中,滴入紫色石蕊试液出现红色,则溶液中离子浓度由大到小的排列顺序为:
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
.(4)A2C2能使酸性KMnO4溶液褪色,该反应的离子方程式为
2MnO4-+5H2O2+6H+=2Mn2++5O2+8H2O
2MnO4-+5H2O2+6H+=2Mn2++5O2+8H2O
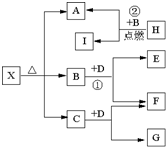
.Ⅱ、已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.试回答下列问题
(1)X、G的化学式分别为:
Mg(HCO3)2
Mg(HCO3)2
、NaOH
NaOH
.(2)B的结构式为
O=C=O
O=C=O
.(3)写出下列反应的化学方程式①
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
②2Mg+CO2
2MgO+C
| ||
2Mg+CO2
2MgO+C
.
| ||