摘要:13.如图是某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图相符合的是 ( ) A.平衡状态I后.增加反应物浓度.达到平衡状态Ⅱ B.平衡状态I后.升高温度.达到平衡状态Ⅱ.由此推知该反应正反应为放热反应 C.平衡状态I后.增大压强.达到平衡状态Ⅱ.由此推知该反应正反应为气体体积缩小的反应 D.平衡状态I后.使用适宜催化剂.达到平衡状态Ⅱ 第Ⅱ卷 第Ⅱ卷用0.5mm的黑色签字笔或黑色墨水钢笔直接答在答题卡上.答在试题卷上无效.
网址:http://m.1010jiajiao.com/timu_id_1745550[举报]
 如图是某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图相符合的是( )
如图是某化学反应的反应速率随反应时间变化的示意图.下列叙述与示意图相符合的是( )| A、平衡状态I后,增加反应物浓度,达到平衡状态Ⅱ | B、平衡状态I后,升高温度,达到平衡状态Ⅱ,由此推知该反应正反应为放热反应 | C、平衡状态I后,增大压强,达到平衡状态Ⅱ,由此推知该反应正反应为气体体积缩小的反应 | D、平衡状态I后,使用适宜催化剂,达到平衡状态Ⅱ |
如图是恒温下某化学反应速率随反应时间变化的示意图。下列叙述与示意图不相符合的是

A.反应达平衡时,正反应速率和逆反应速率相等
B.该反应达到平衡态I后,增大反应物浓度,平衡发生移动,达到平衡态II
C.该反应达到平衡态I后,减小反应物浓度,平衡发生移动,达到平衡态II
D.同一反应物在平衡态I和平衡态II时浓度不相等
查看习题详情和答案>>化学反应与能量有比不可分的关系,回答下列问题.
Ⅰ:已知31g白磷变为31g红磷释放能量.试回答:
(1)上述变化属于
(2)31g白磷具有的能量_
(3)31g白磷完全燃烧释放的能量_
Ⅱ:A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸
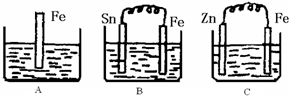
(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A
(2)一段时间后,B中Sn极附近溶液的pH
(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度=
(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
Ⅲ:某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空: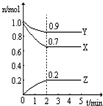
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的
②达平衡时,容器内混合气体的平均相对分子质量比起始投料时
查看习题详情和答案>>
Ⅰ:已知31g白磷变为31g红磷释放能量.试回答:
(1)上述变化属于
化学
化学
(填“物理”或“化学”)变化.(2)31g白磷具有的能量_
>
>
(“>”或“<”)31g红磷具有的能量,常温常压下,红磷
红磷
更稳定.(3)31g白磷完全燃烧释放的能量_
>
>
(“>”或“<”)31g红磷完全燃烧释放的能量.Ⅱ:A、B、C三个烧杯中分别盛有200mL相同物质的量浓度的稀硫酸

(1)分别写出三个装置中铁片表面发生反应的离子方程式:
A
Fe+2H+=Fe2++H2↑
Fe+2H+=Fe2++H2↑
;BFe-2e-═Fe2+
Fe-2e-═Fe2+
;C2H++2e-═H2↑
2H++2e-═H2↑
.(2)一段时间后,B中Sn极附近溶液的pH
pH增大
pH增大
(填“增大”、“减小”、“不变”).(3)一段时间后,C中产生了3.36L(标准状况)气体时,硫酸恰好全部被消耗,则原稀硫酸溶液的物质的量浓度=
0.75
0.75
mol?L-1.此时,三个烧杯中液体质量由大到小的顺序为:C>A=B
C>A=B
(填写序号).(4)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是
BAC
BAC
(填写序号).Ⅲ:某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:

(1)该反应的化学方程式为
3X+Y 2Z
2Z
 2Z
2Z3X+Y 2Z
2Z
. 2Z
2Z(2)反应开始至2min,以气体Z表示的平均反应速率为
0.05mol/(L.min)
0.05mol/(L.min)
.(3)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:
①此时体系的压强是开始时的
0.9
0.9
倍;②达平衡时,容器内混合气体的平均相对分子质量比起始投料时
增大
增大
(填“增大”“减小”或“相等”).如图是部分短周期元素的单质及其化合物(或其溶液)的转化关系,已知B、C、D、E是非金属单质,且在常温常压下都是气体;化合物G的焰色反应为黄色,化合物I和J通常状况下呈气态;

请完成下列填空:
(1)H的化学式______;其晶体中所含化学键类型为______;检验H 中阳离子的方法是______.
(2)A与B 在加热条件下反应的主要现象是______;F和H2O反应的化学方程式为______;写出G溶液中加入过量的I溶液反应的离子方程式______.
(3)某温度时,在2L容器中,D、E、J三种物质的物质的量随时间变化的曲线如图所示.由图中数据分析:该反应的化学方程式为______.反应开始至2min,用J表示的平均反应速率为______.
查看习题详情和答案>>
某化学兴趣小组的同学通过实验比较等体积(200mL)0.55mol/L硫酸、1.1mol/L盐酸、1.1mol/L醋酸分别与过量金属反应生成氢气的速率请你协助完成如下实验,并回答相关问题.

(1)实验用品:仪器(略)、药品(除给定的三种酸溶液外,在Na、Mg、Fe三种金属中选择最合适的一种,并说明理由).选择的金属是______,不选其它两种金属的理由是______.
(2)实验原理:(用离子方程式表示)______.
(3)甲同学设计的实验装置,乙同学认为该装置不能控制三个反应在同一时间发生,并作了相应的改进.你认为乙同学改进的措施是:______.
(4)按改进后的装置进行实验,实验中HCl与金属反应产生H2质量随时间变化的关系见图一,计算实验在80-120s范围内HCl的平均反应速率______(忽略溶液体积变化,写出计算过程).
(5)请在答题卡的框图中,画出HAc、H2SO4与金属反应产生H2质量随时间变化关系的预期结果示意图.
(6)量筒的规格由______决定.
(7)对盐酸和醋酸反应图象的异同,你的解释是______.
查看习题详情和答案>>

(1)实验用品:仪器(略)、药品(除给定的三种酸溶液外,在Na、Mg、Fe三种金属中选择最合适的一种,并说明理由).选择的金属是______,不选其它两种金属的理由是______.
(2)实验原理:(用离子方程式表示)______.
(3)甲同学设计的实验装置,乙同学认为该装置不能控制三个反应在同一时间发生,并作了相应的改进.你认为乙同学改进的措施是:______.
(4)按改进后的装置进行实验,实验中HCl与金属反应产生H2质量随时间变化的关系见图一,计算实验在80-120s范围内HCl的平均反应速率______(忽略溶液体积变化,写出计算过程).
(5)请在答题卡的框图中,画出HAc、H2SO4与金属反应产生H2质量随时间变化关系的预期结果示意图.
(6)量筒的规格由______决定.
(7)对盐酸和醋酸反应图象的异同,你的解释是______.