摘要:27. Ⅰ.氯.溴.碘同在周期表中的第VII A族.在上个世纪.人们很早就制得高碘酸及其盐.但得不到含+7价溴的化合物.1968年.化学家用发现不久的XeF2和KBrO3首先制得纯净的KBrO4 晶体. (1)高碘酸盐(IO65-)能在一定条件下将Mn2+ 氧化为MnO4- .其反应平稳而迅速.写出该离子反应方程式 . (2)在25℃.已知pH=2的高碘酸与pH=12的NaOH溶液等体积混合.所得混合液显酸性,0.01mol/L的碘酸或高锰酸与pH=12的NaOH溶液等体积混合.所得混合液显中性.则高碘酸是 酸,高锰酸是 酸. (3)写出XeF2 和含KOH.KBrO3 的水溶液反应得到KBrO4的离子方程式: . Ⅱ.现有A.B.C.D四种有机物.已知:①它们的相对分子质量都是104 ,②A是芳香烃.B.C.D均为烃的含氧衍生物.分子内均没有甲基,③A.B.C.D能发生如下反应生成高分子化合物X.Y.Z: n A →X .n B → Y + n H2O .n C + n D → Z + 2n H2O .请按要求填空: (1)A 的结构简式是 .A分子中处于同一平面的原子有 个. (2)B发生分子内酯化生成E .其化学反应方程式为 . (3)Z的结构简式是
网址:http://m.1010jiajiao.com/timu_id_1745479[举报]
某化学学习小组设计如图实验装置(夹持装置略去)制备Cl2,并探究氯气的相关性质.
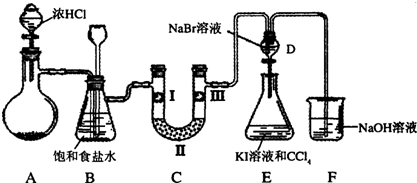
(1)若A装置中固体药品为KClO3,则反应中每生成1mol Cl2时转移电子的物质的量为 mol.
(2)装置B既能除去氯气中的氯化氢,还能检测实验过程中装置C是否发生堵塞.若C中发生堵塞,B中将观察到的现象是 .
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是 .
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.请简述能说明氯、溴、碘非金属性强弱的实验操作及现象 .
(5)请用化学方程式说明装置F的作用 .
(6)甲同学提出,装置F中的试剂可改用足量的Na2SO3溶液,乙同学认真思考后认为此法不可行.请用离子方程式解释乙认为不可行的原因: .
查看习题详情和答案>>

(1)若A装置中固体药品为KClO3,则反应中每生成1mol Cl2时转移电子的物质的量为
(2)装置B既能除去氯气中的氯化氢,还能检测实验过程中装置C是否发生堵塞.若C中发生堵塞,B中将观察到的现象是
(3)装置C的作用是验证氯气是否具有漂白性,l处是湿润的有色布条,则Ⅱ、Ⅲ处应加入的物质分别是
(4)设计装置D、E的目的是比较氯、溴、碘的非金属性.请简述能说明氯、溴、碘非金属性强弱的实验操作及现象
(5)请用化学方程式说明装置F的作用
(6)甲同学提出,装置F中的试剂可改用足量的Na2SO3溶液,乙同学认真思考后认为此法不可行.请用离子方程式解释乙认为不可行的原因:
美国宇航局(NASA)马丽诺娃博士最近找到了一种比二氧化碳有效10 000倍的“超级温室气体”——全氟丙烷,并提出用其“温室化火星”,使火星成为第二个地球的计划。
卤素在有机合成、航天航空工业等许多方面有重要的应用。下列关于氟、氯、溴、碘四种元素的性质递变规律正确的是( )
A.阴离子半径依次增大 B.单质颜色逐渐加深
C.气态氢化物水溶液的酸性依次减弱 D.气态氢化物稳定性增强
查看习题详情和答案>>A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。D、A按原子个数比3∶2形成离子化合物丙。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:(每空2分,共8分)
(1)E元素在周期表中的位置是____________,
(2)画出A的原子结构简图
(3)离子化合物乙的电子式是
(4)C、D、E形成的简单离子半径由大到小的顺序是(用离子符号表示)