网址:http://m.1010jiajiao.com/timu_id_1745284[举报]
A(6分)生活中常用药品很多,如:①碘酒、②麻黄碱、③青霉素、④阿司匹林、⑤葡萄糖注射液、⑥胃舒平(含氢氧化铝、淀粉等)。
⑴上述物质中属于抗生素的是____ _(填写序号,下同),不属于人工合成药物的是 。
⑵胃舒平可防治胃酸分泌过多,其发挥功效时的离子方程式
为 。
⑶药品生产常选用淀粉作填充剂、粘合剂。服用添加淀粉的药物不会伤害身体的原因是_______________________________________________________________。
⑷低血糖病症发作时,喝葡萄糖水可快速见效。葡萄糖作为营养剂供给人体能量,在体内发生的主要反应是_________(填写字母,下同)。
A.加成反应 B.取代反应 C.氧化反应 D.聚合反应
⑸下列关于药物使用的说法中,正确的是__________。
A.碘酒能使蛋白质变性,常用于外敷消毒
B.长期大量服用阿司匹林可预防疾病,没有毒副作用
C.使用青霉素可直接静脉注射,不需进行皮肤敏感试验
D.随着平价药房的开设,生病都可以到药店自己买药服用医治,不用到医院就诊
四、本大题3题,共21分。
查看习题详情和答案>>(本题包括一小题,共12分)
金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(1)Ni原子的核外电子排布式为 ;
(2)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO FeO(填“<”或“>”);
(3)NiO晶胞中Ni和O的配位数分别为 、 ;
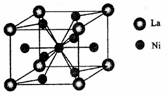
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示。该合金的化学式为 ;
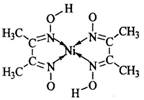
(5)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如右上图所示。
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是 ,氮镍之间形成的化学键是 ;
②该结构中,氧氢之间除共价键外还可存在 ;
③该结构中,碳原子的杂化轨道类型有 。
查看习题详情和答案>>计算题(共10分)
实验室常用的某盐酸试剂瓶的标签上的有关数据如下图,试根据标签上的
有关数据进行计算:
(1)计算该浓盐酸中HCl的
物质的量浓度。
(2)计算欲配制480ml 0.20mol/L的
稀盐酸溶液,需要取上述浓盐酸的体积。
(3)实验室用上述浓盐酸与二氧化锰
反应制取氯气,若制得0.56L
(标准状况)氯气,计算被氧化的 HCl的物质的量及转移电子的物质的量。
查看习题详情和答案>>
计算题(共10分)
实验室常用的某盐酸试剂瓶的标签上的有关数据如下图,试根据标签上的
有关数据进行计算:

(1)计算该浓盐酸中HCl的
物质的量浓度。
(2)计算欲配制480ml 0.20mol/L的
稀盐酸溶液,需要取上述浓盐酸的体积。
(3)实验室用上述浓盐酸与二氧化锰
反应制取氯气,若制得0.56L
(标准状况)氯气,计算被氧化的 HCl的物质的量及转移电子的物质的量。
查看习题详情和答案>>
(10分)已知:(1)2ROH→R-O-R+H2O (R为烃基,R-O-R为醚)
(2)RCH=CH2+HOCl→RCHOH-CH2Cl RCH=CH2+HOCl→RCHCl-CH2OH
试根据下列回答下列问题
(1)写出结构简式A ________________,C ________________。
(2)从结构上分析,可与A互为同分异构体的结构简式有:________________。
(3)上述反应中属于取代反应的是________________________________(填反应序号①②⑧④⑤⑥)
(4)写出方程式:D+E=F________________________________________________________六、(本题包括2d、题,共16分)