摘要:7.将15mL.2mol·L-1Na2CO3溶液逐滴加入到40mLl0.5mol·L-1MCln盐溶液中.恰好将溶液中的Mn+离子沉淀为碳酸盐.则MCln中n值是 A.4 B.3 C.2 D.1
网址:http://m.1010jiajiao.com/timu_id_1745188[举报]
化学试剂的生产和电镀工业排放的废水中常含有20~100mg.L-1Cr(Ⅵ),饮用含Cr(Ⅵ)的水会损害人的肠胃等,已知Cr(Ⅲ)的毒性是Cr(Ⅵ)的0.5%,国家规定工业废水含Cr(Ⅵ)的量排放标准为0.1mg.L-1.工业上常用化学法和电解法处理含Cr(Ⅵ)废水,再将Cr(Ⅲ)转化成沉淀除去,某研究性学习小组为研究废水的净化,设计了如下实验1流程: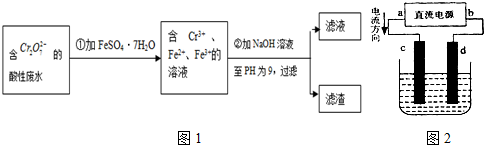
(1)配平第①步反应的离子方程式:
(2)设计一个电解装置也可以实现上述目的,装置如图2(用铁棒和石墨作电极):
电极材料c为:
d极电极反应为:
(3)已知:25℃时Ag2Cr2O7的Ksp=2×10-7.则25℃时,将4×10-2mol?L-1的AgNO3溶液与4×10-4mol?L-1的K2Cr2O7溶液等体积混合
查看习题详情和答案>>

(1)配平第①步反应的离子方程式:
1
1
Cr2O72-+6
6
Fe2++14
14
H+═2
2
Cr3++6
6
Fe3++7
7
H2O
H2O
(2)设计一个电解装置也可以实现上述目的,装置如图2(用铁棒和石墨作电极):
电极材料c为:
铁棒
铁棒
d极电极反应为:
2H2O+2e-=H2↑+2OH-
2H2O+2e-=H2↑+2OH-
(3)已知:25℃时Ag2Cr2O7的Ksp=2×10-7.则25℃时,将4×10-2mol?L-1的AgNO3溶液与4×10-4mol?L-1的K2Cr2O7溶液等体积混合
不能
不能
(填“能”或“不能”) 析出沉淀.