摘要:12.常温下.关于下列溶液的叙述错误的是 ( ) A.pH=3的弱酸溶液和pH =11的强碱溶液等体积混合后溶液呈酸性 B.pH =5的硫酸溶液稀释到原来的500倍.稀释后溶液中c(SO42-)与c(H+)之比约为 1:10 C.向1L0.3mol/L的NaOH溶液缓缓通入CO2气体至溶液增重8.8g.则溶液中 2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)] D.c(NH4+)相等的(NH4)2SO4.(NH4)2CO3.(NH4)2Fe(SO4)2溶液.则 C[(NH4)2SO4]>c[(NH4)2CO3]>c[(NH4)2Fe(SO4)2] 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu_id_1745009[举报]
常温下,关于下列溶液的叙述错误的是
| A.CH3COOH分子可以存在于pH=8的碱性溶液中 |
| B.1mol/L氨水与0.5mol/L氨水中c(OH-)之比是2:1 |
| C.甲酸溶液和一定量NaOH溶液恰好完全反应,溶液中c(HCOO-)<c(Na+) |
| D.等体积等pH的醋酸和盐酸分别加水稀释至a mL和b mL,稀释后溶液pH均为5,则a>b |
常温下,关于下列溶液的叙述错误的是
A.CH3COOH分子可以存在于pH=8的碱性溶液中
B.1mol/L氨水与0.5mol/L氨水中c(OH-)之比是2:1
C.甲酸溶液和一定量NaOH溶液恰好完全反应,溶液中c(HCOO-)<c(Na+)
D.等体积等pH的醋酸和盐酸分别加水稀释至a mL和b mL,稀释后溶液pH均为5,则a>b
查看习题详情和答案>>
常温下,关于下列溶液的叙述错误的是
| A.CH3COOH分子可以存在于pH=8的碱性溶液中 |
| B.1mol/L氨水与0.5mol/L氨水中c(OH-)之比是2:1 |
| C.甲酸溶液和一定量NaOH溶液恰好完全反应,溶液中c(HCOO-)<c(Na+) |
| D.等体积等pH的醋酸和盐酸分别加水稀释至a mL和b mL,稀释后溶液pH均为5,则a>b |
常温下,关于下列溶液的叙述错误的是( )
A.pH=3的弱酸溶液和pH=11的强碱溶液等体积混合后溶液呈酸性
B.pH=5的硫酸溶液稀释到原来的500倍,稀释后溶液中c(SO42-)与c(H+)之比约为1:10
C.向1L0.3mol/L的NaOH溶液缓缓通入CO2气体至溶液增重8.8g,则2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
D.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则c[(NH4)2SO4]>c[(NH4)2CO3]>c[(NH4)2Fe(SO4)2]
查看习题详情和答案>>
A.pH=3的弱酸溶液和pH=11的强碱溶液等体积混合后溶液呈酸性
B.pH=5的硫酸溶液稀释到原来的500倍,稀释后溶液中c(SO42-)与c(H+)之比约为1:10
C.向1L0.3mol/L的NaOH溶液缓缓通入CO2气体至溶液增重8.8g,则2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
D.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则c[(NH4)2SO4]>c[(NH4)2CO3]>c[(NH4)2Fe(SO4)2]
查看习题详情和答案>>
关于下列各图的叙述错误的是 ( )
 |
| 化学方程式 | 平衡常数K |
| F2+H2 | 6.5×1095 |
| Cl2+H2 | 2.6×1033 |
| Br2+H2 | 1.9×1019 |
| I2 + H2 | 8.7×102 |
图 甲 表 乙 图 丙
A.已知1molCO燃烧放出的热为283kJ,2H2(g)+O2(g)=2H2O(g);ΔH= - 483.6kJ/mol则图甲表示CO和H2O(g)生成CO2和H2的能量变化
B.常温下0.4 mol·L-1 HB溶液和0.2 mol·L-1NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(B-)> c(Na+)>c(H+)>c(OH-)
C.常温下,X2(g)和H2反应生成HX的平衡常数如表乙所示,仅依据K的变化,就可以说明在相同条件下,平衡时X2(从F2到I2)的转化率逐减小,且HX的还原性逐渐减弱
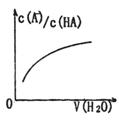
D.图丙中曲线表示常温下向弱酸HA的稀溶液中加水稀释过程中,![]() 的变化情况
的变化情况