摘要:28.氮的化合物在某些领域中扮演着重要的角色. (1)氨和铵盐在粮食的增产中发挥着极其重要的作用.同时又是重要的工业原料. ①写出实验室制取氨气的化学方程式: . ②氨的催化氧化反应是工业制硝酸的基础.该反应在一定温度下为正反应放热的可逆反应.写出该反应的化学平衡常数表达式K= .升高温度.K的值 (填“增大 .“减小 或“不变 ). (2)硝酸是工业三大强酸之一.试从原料的利用率和环境保护两个角度分析.溶解等量的金属铜用浓硝酸好.还是稀硝酸好?写出反应的化学方程式并简要分析 . (3)氮的化合物在航天航空事业中起着不可替代的作用. ①神舟七号飞船的外壳是一种新型结构陶瓷材料.它的主要成分是氮化硅.工业上使用SiCl4.H2和N2在一定条件下反应生成氮化硅.写出该反应的化学方程式 . ②航天发射时.肼(N2H4)及其衍生物常用作火箭推进剂.若以肼为燃料.二氧化氮做氧化剂.两者反应生成氮气和气态水. 已知: 写出肼和二氧化氮反应的热化学方程式 . (4)三聚氰胺[C3N3(NH2)3]是一种重要的有机化工原料.因其含氮量高达而被不法商家用作食品添加剂.以提升食品检测中的蛋白质含量指标(以氮元素的质量分数N%表示).某品牌奶粉中N%为1.9%.若在100g该奶粉中加入10g三聚氰胺.则N%提高为原来的 倍.
网址:http://m.1010jiajiao.com/timu_id_1744414[举报]
 氮的化合物在某些领域中扮演着重要的角色.
氮的化合物在某些领域中扮演着重要的角色.
(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:______;
②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是______(填“强”或“弱”)酸,HA与NH3?H2O恰好完全反应时,混合溶液中由水电离出的c(H+)______(填“>”、“>”或“=”)0.1mol?L-1HA溶液中由水电离出的c(H+);写出C点时混合溶液中各离子浓度由大到小的顺序为______;
(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式______;
(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为______(写离子符号);若反应后无固体剩余,某同学认为X中除Fe3+、Cu2+外还可能含有Fe2+,若要确认其中的Fe2+,应选用______(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.
查看习题详情和答案>>
氮的化合物在某些领域中扮演着重要的角色.
(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:______;
②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是______(填“强”或“弱”)酸,HA与NH3?H2O恰好完全反应时,混合溶液中由水电离出的c(H+)______(填“>”、“>”或“=”)0.1mol?L-1HA溶液中由水电离出的c(H+);写出C点时混合溶液中各离子浓度由大到小的顺序为______;
(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式______;
(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为______(写离子符号);若反应后无固体剩余,某同学认为X中除Fe3+、Cu2+外还可能含有Fe2+,若要确认其中的Fe2+,应选用______(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.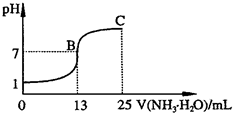
查看习题详情和答案>>
(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:______;
②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是______(填“强”或“弱”)酸,HA与NH3?H2O恰好完全反应时,混合溶液中由水电离出的c(H+)______(填“>”、“>”或“=”)0.1mol?L-1HA溶液中由水电离出的c(H+);写出C点时混合溶液中各离子浓度由大到小的顺序为______;
(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式______;
(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为______(写离子符号);若反应后无固体剩余,某同学认为X中除Fe3+、Cu2+外还可能含有Fe2+,若要确认其中的Fe2+,应选用______(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.

氮的化合物在某些领域中扮演着重要的角色.
(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:______;
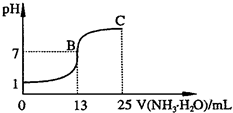
②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是______(填“强”或“弱”)酸,HA与NH3?H2O恰好完全反应时,混合溶液中由水电离出的c(H+)______(填“>”、“>”或“=”)0.1mol?L-1HA溶液中由水电离出的c(H+);写出C点时混合溶液中各离子浓度由大到小的顺序为______;
(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式______;
(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为______(写离子符号);若反应后无固体剩余,某同学认为X中除Fe3+、Cu2+外还可能含有Fe2+,若要确认其中的Fe2+,应选用______(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:______;
②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是______(填“强”或“弱”)酸,HA与NH3?H2O恰好完全反应时,混合溶液中由水电离出的c(H+)______(填“>”、“>”或“=”)0.1mol?L-1HA溶液中由水电离出的c(H+);写出C点时混合溶液中各离子浓度由大到小的顺序为______;
(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式______;
(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为______(写离子符号);若反应后无固体剩余,某同学认为X中除Fe3+、Cu2+外还可能含有Fe2+,若要确认其中的Fe2+,应选用______(选填序号).
a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.
 查看习题详情和答案>>
查看习题详情和答案>>
氮的化合物在某些领域中扮演着重要的角色,其中硝酸是工业的三大强酸之一.
(1)试从原料的利用率和环境保护两个角度分析,
溶解等量的金属铜,用浓硝酸好,还是用稀硝酸好?写出反应的化学方程式并做简要解释:________________.
(2)金属与不同浓度的硝酸反应时,往往生成多种不同价态的还原产物.下图是各种不同密度的硝酸与铁反应时(相同温度)的还原产物分布图.

①某硝酸试剂瓶的标签注明:密度:
1.26 g/mL,质量分数:50.0%.若取该试剂10 mL配成1000 mL溶液,所得溶液的物质的量浓度为________;②当硝酸溶液的密度为
1.36 g/mL时,下列化学方程式中能较准确地表达Fe与过量硝酸反应的是________ (填序号).a.2Fe+10HNO3![]() 2Fe(NO3)3+NO↑+3NO2↑+5H2O
2Fe(NO3)3+NO↑+3NO2↑+5H2O
b.4Fe+18HNO3![]() 4Fe(NO3)3+3NO↑+3NO2↑+9H2O
4Fe(NO3)3+3NO↑+3NO2↑+9H2O
c.2Fe+6HNO3![]() 2Fe(NO3)2+NO↑+NO2↑+3H2O
2Fe(NO3)2+NO↑+NO2↑+3H2O
(3)三聚氰胺[C3N3(NH2)3]是一种重要的有机化工原料,因其含氮量高达66.7%而被不法商家用作食品添加剂,以提升食品检测中的蛋白质含量(以氮元素的质量分数N%表示).某品牌奶粉中N%为1.9%,若在100 g该奶粉中加入10 g三聚氰胺,则N%提高为原来的________倍(取整数).
 (2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.
(2011?青岛模拟)氮的化合物在某些领域中扮演着重要的角色.(1)氨和铵盐在粮食的增产中发挥着极其重要的作用,同时又是重要的工业原料.
①写出实验室制取氨气的化学方程式:
2NH4Cl+Ca(OH)2?CaCl2+2NH3↑+2H2O
2NH4Cl+Ca(OH)2?CaCl2+2NH3↑+2H2O
;②常温下,向25mL 0.1mol?L-1HA溶液中逐滴加入0.2mol?L-1NH3?H2O溶液,曲线如图所示(体积变化忽略不计).由图确定HA是
强
强
(填“强”或“弱”)酸,HA与NH3?H2O恰好完全反应时,混合溶液中由水电离出的c(H+)>
>
(填“>”、“>”或“=”)0.1mol?L-1HA溶液中由水电离出的c(H+);写出C点时混合溶液中各离子浓度由大到小的顺序为c(NH4+)>c(A-)>c(OH-)>c(H+)
c(NH4+)>c(A-)>c(OH-)>c(H+)
;(2)未来的交通工具将采用新一代无机非金属材料制成的无水冷发动机.这类材料中研究得较多的是氮化物A.粉末状A能够与水反应,所得产物中有一种酸性氧化物,它是工业上生产玻璃的主要原料,另一种产物是氨气.请写出A与水反应的化学方程式
Si3N4+6H2O=3SiO2+4NH3↑
Si3N4+6H2O=3SiO2+4NH3↑
;(3)硝酸是医药、军事、化工等领域的重要原料.在实验室中,将适量铁铜混合粉末与稀硝酸充分反应后得到溶液X.若有固体剩余,实验测得溶液X中大量存在的阳离子只有两种,则阳离子为
Fe2+、Cu2+
Fe2+、Cu2+
(写离子符号);若反应后无固体剩余,某同学认为X中除Fe3+、Cu2+外还可能含有Fe2+,若要确认其中的Fe2+,应选用c
c
(选填序号).a.KSCN溶液和氯水 b.铁粉和KSCN溶液 c.酸性KmnO4溶液 d.浓氨水.