网址:http://m.1010jiajiao.com/timu_id_1744275[举报]
A.烧碱溶液注入容器前,需预先煮沸 B.甲电极上有氢气冒出
C.只能用铁作甲电极和乙电极 D.可用食盐水代替烧碱溶液
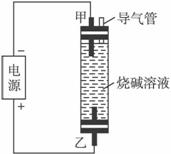
查看习题详情和答案>> 利用如图所示装置制取Fe(OH)2,通电后溶液中产生的白色沉淀能保持较长时间不变色.下列说法错误的是
利用如图所示装置制取Fe(OH)2,通电后溶液中产生的白色沉淀能保持较长时间不变色.下列说法错误的是
- A.只能用铁作甲电极和乙电极
- B.甲电极上有氢气逸出
- C.烧碱溶液注入容器前,需先煮沸
- D.可用食盐水代替烧碱溶液

(1)收集导管B处的气体可采用的方法是
(2)烧杯内放过量稀HNO3的原因是
(3)整个实验过程中,弹簧夹a都必须打开,除为排出产生的气体外,另一个目的是
(4)将烧杯内溶液用蒸发、浓缩、再降温结晶法制得FeCl3?6H2O,而不用直接蒸干的方法来制得晶体的理由是
(5)你认为该实验存在的缺点可能有:
目前工业上有一种用CO2来生产燃料甲醇的方法,可以将CO2变废为宝。
(1)已知在常温常压下:
①2CH3OH(l)+3O2(g)= 2CO2(g)+4H2O(g) △H= _1275.6 kJ·mol-1
②2CO(g)+ O2(g)= 2CO2(g) △H= _556.0 kJ·mol-1
③H2O(l) = H2O(g) △H=+ 44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式 。
(2)某同学利用甲醇燃料电池为电源,设计了一种电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。则电源中a极为 极(填“正”或“负”),其电极反应式为 。装置上端A极电极材料是 (填化学式),B电极上的电极反应式为 。

(3)将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g) +H2O(g) CO2(g) + H2(g),得到如下三组数据:
CO2(g) + H2(g),得到如下三组数据:
|
实验组 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
|
|
H2O |
CO |
CO2 |
|||
|
1 |
650 |
2 |
4 |
1.6 |
5 |
|
2 |
900 |
1 |
2 |
0.4 |
3 |
|
3 |
900 |
1 |
2 |
0.4 |
1 |
①该反应的正反应为 (填“吸”或“放”)热反应。
②实验1中,以v(H2)表示的平均反应速率为 。
③900℃时,按CO(g)、H2O(g)、CO2(g) 和 H2(g)的物质的量分别是0.8mol、1.0mol、0.6 mol和0.8 mol分别加入该容器,则此时反应的v(正) v(逆)(填“>”“<”或“=”中之一)。
④实验3跟实验2相比,改变的条件可能是 。
查看习题详情和答案>>
 利用如图所示装置制取Fe(OH)2,通电后溶液中产生的白色沉淀能保持较长时间不变色.下列说法错误的是( )
利用如图所示装置制取Fe(OH)2,通电后溶液中产生的白色沉淀能保持较长时间不变色.下列说法错误的是( )