摘要:13.下图是798K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( ) A.该反应的热化学方程式为:N2+3H2 2NH3,△H=-92kJ·mol-1 B.b曲线是加入铁触媒时的能量变化曲线 C.加入铁触媒.该化学反应的反应热改变 D.加入铁触媒可增大正反应速率.降低逆反应速率.反应物的转化率提高 II卷
网址:http://m.1010jiajiao.com/timu_id_1744110[举报]
下图是298K时N2与H2反应过程中能量变化的曲线图。

下列叙述正确的是( )
A 该反应的热化学方程式为:N2+3H2  2NH3,△H=-92 kJ·mol-1
2NH3,△H=-92 kJ·mol-1
B a曲线是加入正催化剂时的能量变化曲线
C 加入催化剂,该化学反应的反应热改变
D 在温度、体积一定的条件下,通入1mol N2和3mol H2,,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2,反应后放出的热量为Q2 kJ,则184 > Q2 > 2Q1
查看习题详情和答案>>
下图是298K时N2与H2反应过程中能量变化的曲线图。
下列叙述正确的是( )
A 该反应的热化学方程式为:N2+3H2  2NH3,△H=-92 kJ·mol-1
2NH3,△H=-92 kJ·mol-1
B a曲线是加入正催化剂时的能量变化曲线
C 加入催化剂,该化学反应的反应热改变
D 在温度、体积一定的条件下,通入1mol N2和3mol H2,,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2,反应后放出的热量为Q2 kJ,则184 > Q2 > 2Q1
下图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是
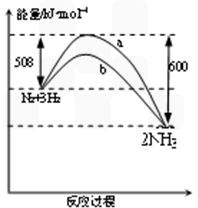
[ ]
A. 该反应的热化学方程式为: N2(g) + 3H2(g) 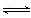 2NH3(g) ΔH = 92kJ·mol-1
2NH3(g) ΔH = 92kJ·mol-1
B.b曲线是升高温度时的能量变化曲线
C. 加入催化剂, 该化学反应的活化能和反应热都改变
D. 在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
查看习题详情和答案>>
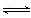 2NH3(g) ΔH = 92kJ·mol-1
2NH3(g) ΔH = 92kJ·mol-1 B.b曲线是升高温度时的能量变化曲线
C. 加入催化剂, 该化学反应的活化能和反应热都改变
D. 在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
 如图是778K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )
如图是778K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是( )