摘要:某化学兴趣小组同学用实验室中一瓶久置的NaOH固体做了以下实验:先称取13.3gNaOH样品(杂质为Na2CO3).配成溶液.然后向溶液中逐滴加入浓度为4mol/L的盐酸.再根据生成的CO2体积计算出Na2CO3质量.从而进一步计算出样品中变质NaOH的质量. 请回答下列问题: (1)该实验的目的是 . (2)已知20℃时.Na2CO3溶解度为21.7g.NaOH溶解度为108.3g.若要将所称取的样品恰好溶解.最多需要蒸馏水 g.溶解样品所需的仪器是 . (3)实验测得加入盐酸的体积与产生CO2的体积关系如下图所示: 则13.3g该样中未变质的NaOH的质量为 ,NaOH的变质程度为 ,与NaOH反应消耗的盐酸体积为 mL. (4)根据“与NaOH反应消耗盐酸的体积 .并对照上述图象.他们从实验中还发现了什么问题? .并由此得出了什么结论? .
网址:http://m.1010jiajiao.com/timu_id_1743680[举报]
(2011?武汉模拟)某化学兴趣小组的同学通过査阅资料,获得了草酸的一些信息,整理出下表:
(1)该组同学欲通过实验验证草酸受热分解产物中的CO2和CO(装置符合气密性要求,其它试剂可自选).
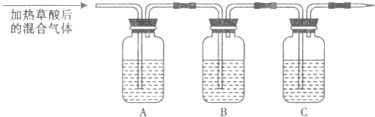
①填写表中空白.
②简述检验CO的实验方法和实验现象.
(2)实验室常用草酸钠测定KMnO4溶液的浓度.
①准确称取2.680g草酸钠,溶于稀硫酸和水制成100.0mL溶液,每次取20.00mL溶液于锥形瓶中;将待测KMnO4溶液置于
待测KMnO4溶液的物质的量浓度为
②将酸性高锰酸钾溶液和草酸溶液混合后,发现开始时溶液褪色不明显,但不久迅速褪色.针对该实验现象,某同学认为KMnO4溶液与H2C2O4溶液反应是放热反应,导致溶液温度升高,反应速率加快.你猜想还有可能是
查看习题详情和答案>>
| 结构简式 | HOOH-COOH | |||
| 溶解性 | 能溶于水,易溶于乙醇 | |||
| 特性 | 大约在157℃升华(175℃以上发生分解) | |||
| 化学性质 | H2C2O4+Ca(OH)2═CaC2O4↓+2H2O | |||
HOOC-COOH
| ||||
| 2KMnO4+5H2C2O4+3H2SO4═KSO4+2MnSO4+10CO2↑2O |

①填写表中空白.
| 仪器 | A | B | C |
| 加入试剂 | NaOH溶液 |
在C处后尖嘴管点燃气体,火焰呈蓝色,再用一个内壁附着澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊
在C处后尖嘴管点燃气体,火焰呈蓝色,再用一个内壁附着澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊
(2)实验室常用草酸钠测定KMnO4溶液的浓度.
①准确称取2.680g草酸钠,溶于稀硫酸和水制成100.0mL溶液,每次取20.00mL溶液于锥形瓶中;将待测KMnO4溶液置于
酸式
酸式
(填“酸式”或“碱式“)滴定管中进行滴定.重复上述滴定操作三次,实验数据如表所示.| 滴定前均为 | 第一次终点 | 第二次终点 | 第三次终点 | |
| 滴定管液面刻度 | 0.00mL | 20.02mL | 21.00mL | 19.98mL |
0.08000 mol/L
0.08000 mol/L
.②将酸性高锰酸钾溶液和草酸溶液混合后,发现开始时溶液褪色不明显,但不久迅速褪色.针对该实验现象,某同学认为KMnO4溶液与H2C2O4溶液反应是放热反应,导致溶液温度升高,反应速率加快.你猜想还有可能是
催化剂(或Mn2+的催化作用)
催化剂(或Mn2+的催化作用)
的影响.若用实验证明你的猜想,除高锰酸钾溶液、草酸溶液、稀硫酸外,还需要选择的合理试剂是硫酸锰(或MnSO4)
硫酸锰(或MnSO4)
.