摘要:对于反应:N2(g)+ 3H2(g)2NH3(g),ΔH<0.在一定条件下使该反应达平衡.下列叙述中错误的是 A.若分离出部分NH3后.正反应速率将变小 B.若增加H2的量.N2的转化率将变大 C.若保持温度不变.减小压强.达新平衡时.N2.H2.NH3的浓度均减小 D.若保持压强不变.升高温度.达新平衡后.混合气体的平均分子量变大
网址:http://m.1010jiajiao.com/timu_id_1743675[举报]
对于反应:N2(g)+O2(g) 2NO(g),在密闭容器中进行,下列条件能使反应速率减小的是
2NO(g),在密闭容器中进行,下列条件能使反应速率减小的是
 2NO(g),在密闭容器中进行,下列条件能使反应速率减小的是
2NO(g),在密闭容器中进行,下列条件能使反应速率减小的是 [ ]
A.缩小体系体积
B.体系体积不变,充入N2
C.体系体积不变,充入He
D.体系压强不变,充入气体Ne
查看习题详情和答案>>
B.体系体积不变,充入N2
C.体系体积不变,充入He
D.体系压强不变,充入气体Ne
对于反应:N2(g)+O2(g) 2NO(g),在密闭容器中进行,下列条件能加快其反应速率的是
2NO(g),在密闭容器中进行,下列条件能加快其反应速率的是
 2NO(g),在密闭容器中进行,下列条件能加快其反应速率的是
2NO(g),在密闭容器中进行,下列条件能加快其反应速率的是[ ]
A.缩小体积使压强增大
B.体积不变,充入N2使压强增大
C.体积不变,充入He使气体压强增大
D.总压强不变,充入Ne
查看习题详情和答案>>
B.体积不变,充入N2使压强增大
C.体积不变,充入He使气体压强增大
D.总压强不变,充入Ne
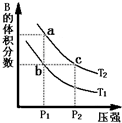 对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.
对于反应A(g)?2B(g)△H>0,在温度为T1、T2时,平衡体系中B的体积分数随压强变化的曲线如图所示.回答下列各题.(1)根据曲线图,分析下列说法正确的是
BC
BC
(填字母).A.a、c两点的反应速率:a>c
B.由状态b到状态a,可以通过加热的方法
C.b、c两点A气体的转化率相等
(2)上述反应在密闭容器(定容)中进行,达到平衡状态的标志是
BE
BE
(填字母).A.单位时间内生成n mol A的同时分解2n molB
B.两种气体的体积分数不再改变
C.v正(A)=2v逆(B)
D.混合气体的密度不再发生变化
E.混合气体的压强不再发生变化
(3)若上述反应达平衡时,B气体的平衡浓度为0.1mol?L-1,通过减小体积来增大体系的压强(温度保持不变),重新达平衡后,B气体的平衡浓度
>
>
0.1mol?L-1(填“>”、“<”或“=”).(4)在100℃时,将0.40mol的B气体充入2L抽空的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到如下表的数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(B)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(A)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
0.000875mol/(L?s)
0.000875mol/(L?s)
;②上表中n3
=
=
n4(填“>”、“<”或“=”),反应A(g)?2B(g)在100℃时的平衡常数K的值为0.36
0.36
,升高温度后,反应2B(g)?A(g)的平衡常数K的值减小
减小
(填“增大”、“减小”或“不变”);③若在相同情况下最初向该容器中充入的是A气体,要达到上述同样的平衡状态,A气体的起始浓度为
0.1
0.1
mol?L-1.