摘要:27.有一化合物X.其水溶液为浅绿色.可发生如下的转化关系(部分反应物.生成物从略).其中B.D.E.F均为无色气体.M.L为常见的金属单质.C为难溶于水的红褐色固体.在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀.H和M反应可放出大量的热.请回答下列问题: (1)B的电子式为 .B气体的检验方法为 . (2)电解混合液时阳极反应式为 . (3)按要求写出上述转化关系中有关反应的化学方程式: ①含有L元素的化合反应: . ②含有L元素的置换反应: . (4)L与过量G的稀溶液反应的离子方程式为: . (5)物质X的化学式为 . (6)已知a g E气体在D中完全燃烧生成稳定的化合物时.放出b KJ的热量.写出E燃烧热的热化学方程式: .
网址:http://m.1010jiajiao.com/timu_id_1743198[举报]
有一化合物X(不含结晶水),其水溶液为浅绿色,可发生如下的转化关系(部分反应物,生成物已略).其中B、D、E、F均为无色气体.M、L为常见的金属单质,C为难溶于水的红褐色固体.在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和M反应可放出大量的热.
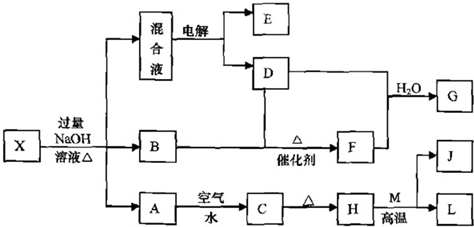
请回答下列问题:
(1)B物质的电子式为 ;B气体的检验方法为 .
(2)按要求写出上述转化关系中有关反应的化学方程式:
①含有L元素的化合反应: ;
②含有L元素的置换反应: .
(3)L与过量C的稀溶液反应的离子方程式为 .
(4)物质X的化学式为 .
(5)物质X溶于水结晶析出晶体的组成可表示为X?nH2O,为测定n.称取WgX?nH2O晶体溶于水中,配制100mL溶液,再用滴定管取出10.00mL,用Cmol?L-l的酸性KMnO4溶液进行滴定,滴定所发生反应为:5L2++MnO4-+8H+=5L3++Mn2++4H2O达到滴定终点时,共用酸性KMnO4溶液VmL,则所配X溶液的溶质的物质的量浓度为 mol?L-1,由此算出X?nH2O晶体中结晶水的n值是 (以上答案用字母表示).
查看习题详情和答案>>

请回答下列问题:
(1)B物质的电子式为
(2)按要求写出上述转化关系中有关反应的化学方程式:
①含有L元素的化合反应:
②含有L元素的置换反应:
(3)L与过量C的稀溶液反应的离子方程式为
(4)物质X的化学式为
(5)物质X溶于水结晶析出晶体的组成可表示为X?nH2O,为测定n.称取WgX?nH2O晶体溶于水中,配制100mL溶液,再用滴定管取出10.00mL,用Cmol?L-l的酸性KMnO4溶液进行滴定,滴定所发生反应为:5L2++MnO4-+8H+=5L3++Mn2++4H2O达到滴定终点时,共用酸性KMnO4溶液VmL,则所配X溶液的溶质的物质的量浓度为