摘要:32.[化学-物质结构与性质] 下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素 试回答下列问题: (1)元素f的基态原子电子排布式 (2)a与c形成的化合物.其分子够型为 .中心原子的杂化形式为 . (3)由b原子跟d原子以1:1相互交替结合而形成的晶体.晶型与晶体d相同.但其熔点比晶体d高.原因为: (4)1183K以下e晶体的基本结构单元如图1所示.1183K以上转变为图2所示结构的基本结构单元.在两种晶体中最邻近的e的原子间距离相同. ①在1183K以下的晶体中.与e原子等距离且最近的原子数为 个,在1183K以上的晶体中.与e原子等距离且最近的原子数为 , ②转变温度前后两者的密度比(1183K以下与1183K以上之比) .
网址:http://m.1010jiajiao.com/timu_id_1743059[举报]
[物质结构与性质]下表是元素周期表的一部分.表中所列的字母分别代表一种化学元素.

试回答下列问题:
(1)请写出元素o的基态原子电子排布式 .
(2)d的氢化物中心原子的杂化方式是 .
(3)c、e、k三种元素的电负性数值由小到大的顺序为 (用元素符号作答).
(4)f、l、q的氢化物中沸点最高的是 (写化学式)
(5)j原子形成的晶体与j原子跟c原子以1:1相互交替结合而形成的jc晶体类型相同.则j晶体的熔点 jc晶体的熔点(填“大于”“等于”“小于”)原因是: .
查看习题详情和答案>>

试回答下列问题:
(1)请写出元素o的基态原子电子排布式
(2)d的氢化物中心原子的杂化方式是
(3)c、e、k三种元素的电负性数值由小到大的顺序为
(4)f、l、q的氢化物中沸点最高的是
(5)j原子形成的晶体与j原子跟c原子以1:1相互交替结合而形成的jc晶体类型相同.则j晶体的熔点
(物质结构与性质)下表是元素周期表的一部分.表中所列的字母分别代表某一化学元素.

(1)下列________(填写编号)组元素的单质可能都是电的良导体.
①a、c、h
②b、g、k
③c、h、1
④d、e、m
(2)如果给核外电子足够的能量,这些电子便会摆脱原子核的束缚而离去.核外电子离开该原子或离子所需要的能量主要受两大因素的影响:
1.原子核对核外电子的吸引力
2.形成稳定结构的倾向
下表是一些气态原子失去核外不同电子所需的能量(kJ·mol-1):

①通过上述信息和表中的数据分析为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量.________.
②表中X可能为以上13种元素中的________(填写字母)元素.用元素符号表示X和j形成化合物的化学式________.
③Y是周期表中________族元素.
④以上13种元素中,________(填写字母)元素原子失去核外第一个电子需要的能量最多
[三选一----物质结构与性质]
下表为元素周期表的一部分,其中编号代表对应的元素。
下表为元素周期表的一部分,其中编号代表对应的元素。

请回答下列问题:
(1)写出元素⑥的基态原子电子排布式__________,元素⑦位于_____________区。
(2)元素②和③的第一电离能大小顺序是__________(用元素符号表示)。请写出由第二周期元素组成的与N3-互为等电子体的离子的化学式_________ ,其空间立体结构为___________。
(3)在测定①和④形成的化合物的相对分子质量时,实验测得值一般高于理论值,其主要原因是____________。
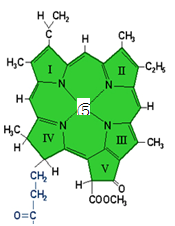
(4)在叶绿素a中含有元素⑤,下图是叶绿素a的部分结构,在该分子中C原子的杂化类型有___________。
(1)写出元素⑥的基态原子电子排布式__________,元素⑦位于_____________区。
(2)元素②和③的第一电离能大小顺序是__________(用元素符号表示)。请写出由第二周期元素组成的与N3-互为等电子体的离子的化学式_________ ,其空间立体结构为___________。
(3)在测定①和④形成的化合物的相对分子质量时,实验测得值一般高于理论值,其主要原因是____________。
(4)在叶绿素a中含有元素⑤,下图是叶绿素a的部分结构,在该分子中C原子的杂化类型有___________。
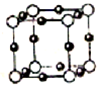
(5)②和⑦形成某种化合物的晶胞结构如上图所示(每个球均表示1个原子,其中②显-3价),则其化学式为________________。
查看习题详情和答案>>
[物质结构与性质](15分)
下表为长式周期表的一部分,其中的序号代表对应的元素。
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | ⑥ | |
| | ⑦ | | | | | | | | | | | | | | | ⑧ | |
| | | | | | ⑨ | | | | | ⑩ | | | | | | | |
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为__________杂化;元素⑦与⑧形成的化合物的晶体类型是__________。
(3)元素④的第一电离能__________元素⑤(填写“>”“=”或“<”)的第一电离能;元素④与元素①形成的最简单的X分子的空间构型为__________。请写出与元素④的单质互为等电子体分子、离子的化学式__________(各写一种)。
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______。
(5)元素④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式为__________。
(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,反应的离子方程式为__________;元素⑩的某种氧化物的晶体结构如图所示,其中实心球表示元素⑩原子,则一个晶胞中所包含的氧原子数目为__________。
 查看习题详情和答案>>
查看习题详情和答案>>
[物质结构与性质](15分)
下表为长式周期表的一部分,其中的序号代表对应的元素。
(1)写出上表中元素⑨原子的外围电子排布式__________。
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为__________杂化;元素⑦与⑧形成的化合物的晶体类型是__________。
(3)元素④的第一电离能__________元素⑤(填写“>”“=”或“<”)的第一电离能;元素④与元素①形成的最简单的X分子的空间构型为__________。请写出与元素④的单质互为等电子体分子、离子的化学式__________(各写一种)。
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______。
(5)元素④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式为__________。
(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,反应的离子方程式为__________;元素⑩的某种氧化物的晶体结构如图所示,其中实心球表示元素⑩原子,则一个晶胞中所包含的氧原子数目为__________。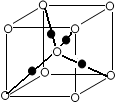
下表为长式周期表的一部分,其中的序号代表对应的元素。
| ① | | | | | | | | | | | | | | | | | |
| | ② | | | | | | | | | | | | ③ | ④ | ⑤ | ⑥ | |
| | ⑦ | | | | | | | | | | | | | | | ⑧ | |
| | | | | | ⑨ | | | | | ⑩ | | | | | | | |
(2)在元素③与①形成的水果催熟剂气体化合物中,元素③的杂化方式为__________杂化;元素⑦与⑧形成的化合物的晶体类型是__________。
(3)元素④的第一电离能__________元素⑤(填写“>”“=”或“<”)的第一电离能;元素④与元素①形成的最简单的X分子的空间构型为__________。请写出与元素④的单质互为等电子体分子、离子的化学式__________(各写一种)。
(4)在测定元素①与⑥形成化合物的相对分子质量时,实验测得的值一般高于理论值的主要原因是_______。
(5)元素④的最高价氧化物对应的水化物稀溶液与元素⑦的单质反应时,元素④被还原到最低价,该反应的化学方程式为__________。
(6)将过量的X通入含有元素⑩的蓝色硫酸盐溶液中,反应的离子方程式为__________;元素⑩的某种氧化物的晶体结构如图所示,其中实心球表示元素⑩原子,则一个晶胞中所包含的氧原子数目为__________。
