摘要:18.将一定质量的Mg和Al的混合物投入1 mol·L-1500mL稀硫酸中.固体全部溶解并产 生气体.待反应完全后.向所得溶液中加入NaOH溶液.生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是 ( ) A.Mg和Al的物质的量之比1:1 B.NaOH溶液的物质的量浓度为5 mol·L-1 C.生成的H2在标准状况下的体积为11.2L D.Mg和Al和硫酸恰好完全反应 第Ⅱ卷 非选择题(本题包括6小 题.共46分)
网址:http://m.1010jiajiao.com/timu_id_1743029[举报]
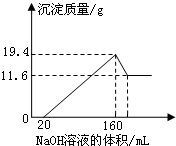 将一定质量的镁铝合金样品全部溶于100mL某浓度的盐酸中.向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如图所示.求:
将一定质量的镁铝合金样品全部溶于100mL某浓度的盐酸中.向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如图所示.求:(1)写出图中每个阶段的离子反应方程式,0至20mL
H++OH-═H2O
H++OH-═H2O
,20mL至160mL时,Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓
Mg2++2OH-═Mg(OH)2↓、Al3++3OH-═Al(OH)3↓
,160mL至V1 mL时,Al(OH)3+OH-═AlO2-+2H2O
Al(OH)3+OH-═AlO2-+2H2O
.(2)合金中Mg和Al的质量分别为多少克?(写出计算过程)
(3)盐酸的物质的量浓度是多少?
 (2009?长春一模)将一定质量的Mg和Al的混合物投入1mol?L-1500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
(2009?长春一模)将一定质量的Mg和Al的混合物投入1mol?L-1500mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.则下列说法正确的是( )
查看习题详情和答案>>
 将一定质量的Mg和Al混合物投入400mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.计算:
将一定质量的Mg和Al混合物投入400mL稀硫酸中,固体全部溶解并产生气体.待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如图所示.计算:(1)Mg和Al的总质量为多少g?
(2)硫酸的物质的量浓度为多少?
(3)生成的H2物质的量为多少?
(2009?深圳二模)氯碱厂废渣(盐泥)中含有镁钙铁铝的硅酸盐和碳酸盐,其中含镁(以MgO计)约10%,钙(以CaO计)约15%,铁(Ⅱ、Ⅲ)和铝等的含量低于1%.氯碱厂从盐泥中提取MgSO4.7H2O的流程如下:
部分阳离子以氢氧化物沉淀时溶液pH
溶解度表
回答下列问题: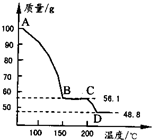
(1)滤渣B的主要成分是:
(2)从滤液A得到滤液C,能否用氨水代替NaClO?
(3)从滤液C中获得产品经过3个操作步骤,分别是
(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式
查看习题详情和答案>>

部分阳离子以氢氧化物沉淀时溶液pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 11.2 |
| 温度0C | 10 | 30 | 40 |
| CaSO4 | 0.19 | 0.21 | 0.21 |

(1)滤渣B的主要成分是:
H2SiO3(或H4SO4)\CaSO4(或CaSO4?2H2O)
H2SiO3(或H4SO4)\CaSO4(或CaSO4?2H2O)
.(2)从滤液A得到滤液C,能否用氨水代替NaClO?
否
否
,什么理由氨水不能将Fe2+氧化成Fe3+,则无法沉淀完全
氨水不能将Fe2+氧化成Fe3+,则无法沉淀完全
,其中加热煮沸的目的是加热能使Fe3+和Al3+水解完全,同时因为氢氧化铁和氢氧化铝是胶状沉淀,加热有利于破坏胶体的稳定性,使沉淀颗粒变大利于后面过滤分离
加热能使Fe3+和Al3+水解完全,同时因为氢氧化铁和氢氧化铝是胶状沉淀,加热有利于破坏胶体的稳定性,使沉淀颗粒变大利于后面过滤分离
.(3)从滤液C中获得产品经过3个操作步骤,分别是
加热浓缩
加热浓缩
,冷却结晶
冷却结晶
,过滤
过滤
.(4)将一定质量的MgSO4.7H2O放在坩埚中加热测得不同温度阶段剩余固体质量如图所示.
据图写出CD段反应的化学方程式
MgSO4?H2O
MgSO4+H2O↑
| ||
MgSO4?H2O
MgSO4+H2O↑
.
| ||
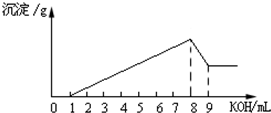 将一定质量的Mg-Al合金用稀盐酸全部溶解,向所得溶液中滴加KOH溶液的体积与生成的沉淀质量关系如图所示.则合金中Al和Mg的物质的量之比为( )
将一定质量的Mg-Al合金用稀盐酸全部溶解,向所得溶液中滴加KOH溶液的体积与生成的沉淀质量关系如图所示.则合金中Al和Mg的物质的量之比为( )