摘要:28.现有A.B.C.D.E.F六种周期元素.它们的原子序数依次增大.A.D同主族.C.E同主族.D.E.F同周期.A.B的原子最外层电子数之和与C原子的最外层电子数相等.A能分别与B.C形成电子总数相等的分子.且A与C形成常见化合物常温下为液态.A能分别与E.F形成电子总数相等的常温下为气体的分子. 请回答下列问题: (1)A-F六种元素原子.原子半径最大的是 (填对应的元素符号.下同) (2)A与B两种元素组成一种阳离子.该离子的检验方法为 a.取含有该离子的溶液与强碱溶液共热.若放出能使湿润的红色石蕊试纸变蓝的气体.则证明有该离子 b.取含有该离子的盐固体与碱石灰共热.产生能使湿润的红色石蕊试纸变蓝的气体.则证明有该离子 c.加热含有该离子的盐溶液.产生能使湿润的红色石蕊试纸变蓝的气体.则证明有该离子 (3)C.D两种元素组成的化合物中.既含有离子键.又含有非极性共价键.该化合物的电子式为 , (4)E.F两种元素中非金属性较强的是 .能够证明这一结论的一个化学事实是 . (5)写出电解由D.F两种元素组成的化合物的水溶液的化学方程式: ,该电解槽可否用铁作阳极 .
网址:http://m.1010jiajiao.com/timu_id_1742820[举报]
 现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.
现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E同主族,且D的氢化物常温时为液态.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子.(1)C的元素符号是
N
N
;B的最高价氧化物的电子式为

第三周期第ⅦA族
第三周期第ⅦA族
.(2)B、C、D元素的氢化物的沸点由商到低的顺序为
H2O>NH3>CH4
H2O>NH3>CH4
(用化学式表示).(3)将足量D的单质通入到A2E的溶液中,反应的化学方程式为
2H2S+O2=2S↓+2H2O
2H2S+O2=2S↓+2H2O
(4)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4气态分子.C4分子结构如图所示,已知断裂1molC-C吸收l67KJ的热量,生成1mol C≡C放出942KJ热量.试写出由C4气态分子变成C2气态分子的热化学方程式:
N4(g)=2N2(g)△H=-882kJ/mol
N4(g)=2N2(g)△H=-882kJ/mol
.(5)某盐x(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.
①盐x显酸性原因(用离子方程式表示)
N2H62++H2O?[N2H5?H2O]++H+
N2H62++H2O?[N2H5?H2O]++H+
.②写出足量金属镁加入盐x的溶液中产生H2的记学方程式为
Mg+N2H6Cl2=MgCl2+N2H4+H2↑
Mg+N2H6Cl2=MgCl2+N2H4+H2↑
.现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.室温下E元素的单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜;D元素原子核外M电子层与K电子层上的电子数相等;A可分别与B、F形成A2B,A2B2、AF等共价化合物;C可分别与B、F形成C2B、C2B2、CF等离子化合物.
请回答下列问题:
(1)以上六种元素中,金属性最强的是(填元素符号)
 .
.
(2)以上元素形成的简单离子中,核外电子数相等的是(填真实的离子符号)
(3)C2B2的电子式为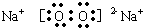
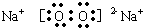 ,该物质中存在的化学键有
,该物质中存在的化学键有
(4)A2B与C2B2反应的化学方程式是
查看习题详情和答案>>
请回答下列问题:
(1)以上六种元素中,金属性最强的是(填元素符号)
Na
Na
,F原子的结构示意图为

(2)以上元素形成的简单离子中,核外电子数相等的是(填真实的离子符号)
O2-、Na+、Mg2+、Al3+
O2-、Na+、Mg2+、Al3+
.(3)C2B2的电子式为
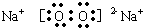
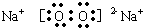
离子键、非极性键(或共价键)
离子键、非极性键(或共价键)
.(4)A2B与C2B2反应的化学方程式是
2H2O+2Na2O2=4NaOH+O2↑
2H2O+2Na2O2=4NaOH+O2↑
.现有A、B、C、D、E、F六种短周期元素,原子序数依次增大.已知A与D、C与E分别同主族,D、E、F同周期;A、B的最外层电子数之和与C的最外层电子数相等,A与C形成的化合物常温下均为液态,A分别与E、F形成的气体分子电子总数相等.
请回答下列问题:
(1)元素B在周期表中的位置是
 .
.
(2)A2C比A2E沸点高的原因是
(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为
(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为
查看习题详情和答案>>
请回答下列问题:
(1)元素B在周期表中的位置是
第二周期第ⅤA族
第二周期第ⅤA族
,元素D的原子结构示意图为

(2)A2C比A2E沸点高的原因是
H2O分子间存在氢键而H2S分子间不能形成氢键
H2O分子间存在氢键而H2S分子间不能形成氢键
.(3)在一定条件下,A、C的单质和A、C、D形成的离子化合物的水溶液可构成电池,该电池正极的电极反应式为
O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
,负极的电极反应式为2H2+4OH--4e-═4H2O
2H2+4OH--4e-═4H2O
,该电池在放电过程中,电解质溶液的pH将减小
减小
(填“增大”、“减小”或“不变”).(4)化合物B2A4和B2C4的液体曾被用作火箭推进剂,燃烧反应的生成物是一种气态单质和一种化合物,它们对环境无污染.1mol B2A4与B2C4完全反应生成两种气体时放出热量516.8kJ,则该反应的热化学方程式为
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H=-1033.6kJ?mol-1
2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H=-1033.6kJ?mol-1
.现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子甲、乙、丙.
(1)元素F在周期表中的位置是
(2)写出元素A、C形成分子C2A4的电子式:
 .
.
(3)甲、乙、丙三物质沸点由高到低的顺序为(用分子式):
(4)生活中的一种绿色氧化剂由A和D组成,一定条件下也可表现出还原性,试写出其和酸性KMnO4反应的离子方程式:
(5)某盐X(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.盐X显酸性原因(用离子方程式表示)
查看习题详情和答案>>
(1)元素F在周期表中的位置是
第三周期第ⅦA族
第三周期第ⅦA族
.(2)写出元素A、C形成分子C2A4的电子式:


(3)甲、乙、丙三物质沸点由高到低的顺序为(用分子式):
H2O>NH3>CH4
H2O>NH3>CH4
.(4)生活中的一种绿色氧化剂由A和D组成,一定条件下也可表现出还原性,试写出其和酸性KMnO4反应的离子方程式:
2MnO4-+5H2O2+16H+=2Mn2++5O2↑+8H2O
2MnO4-+5H2O2+16H+=2Mn2++5O2↑+8H2O
.(5)某盐X(C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性.盐X显酸性原因(用离子方程式表示)
N2H62++H2O?[N2H5?H2O]++H+
N2H62++H2O?[N2H5?H2O]++H+
.现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,A、D同主族,C与E同主族,D、E、F同周期,A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C形成电子总数相等的分子,且A与C形成的化合物常温下为液态,A能分别与E、F形成电子总数相等的气体分子.
请回答下列问题:
(1)E、F气态氢化物的稳定性为
(2)E与F可形成E2F2的化合物,其电子式为
 ,其晶体类型为
,其晶体类型为
(3)C、D形成的一种化合物能与D、E形成的化合物在溶液中发生氧化还原反应,其离子方程式为:
(4)A、C、E三种元素形成的一种常见化合物H,其浓溶液在加热条件下可与a g铜反应,则被还原的H的物质的量为
mol
mol.
(5)E的一种常见氧化物为大气污染物,实验室可用足量D的最高价氧化物的水化物来吸收,则吸收生成的盐溶液中离子浓度大小关系为:
(6)b g D单质在纯净的C单质中燃烧放出Q kJ热量,则相关的热化学方程式为:
查看习题详情和答案>>
请回答下列问题:
(1)E、F气态氢化物的稳定性为
HCl
HCl
>H2S
H2S
(用化学式表示).(2)E与F可形成E2F2的化合物,其电子式为


分子晶体
分子晶体
.(3)C、D形成的一种化合物能与D、E形成的化合物在溶液中发生氧化还原反应,其离子方程式为:
Na2O2+S2-+2H2O=S↓+2Na++4OH-
Na2O2+S2-+2H2O=S↓+2Na++4OH-
.(4)A、C、E三种元素形成的一种常见化合物H,其浓溶液在加热条件下可与a g铜反应,则被还原的H的物质的量为
| a |
| 64 |
| a |
| 64 |
(5)E的一种常见氧化物为大气污染物,实验室可用足量D的最高价氧化物的水化物来吸收,则吸收生成的盐溶液中离子浓度大小关系为:
c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)
.(6)b g D单质在纯净的C单质中燃烧放出Q kJ热量,则相关的热化学方程式为:
2Na(s)+O2(g)=Na2O2(s)△H=-
kJ/mol
| 46Q |
| b |
2Na(s)+O2(g)=Na2O2(s)△H=-
kJ/mol
.| 46Q |
| b |