摘要:15.肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构.它的沸点高达l13℃.燃烧热为642 kJ·mol-1.肼与氧气及氢氧化钾溶液还可构成燃料电池.已知肼的球棍模型如图所示.下列有关说法正确的是 ( ) A.肼是由极性键和非极性键构成的非极性分子 B.肼沸点高达l13℃.可推测肼分子间可形成氢键 C.肼燃烧的热化学方程式为:N2H4(g)+O2(g) = N2(g) +2H2O(g), △H=-642 kJ·mol-1 D.肼-氧气燃料电池.负极的电极反应为:O2 +2H2O+4e-=4OH- 2,4,6 第Ⅱ卷(必做120分+选做32分.共152分) 20090316 1.第II卷共15小题.其中23-30题为必做部分.31-37题为选做部分.考生必须从中选择2个物理.1个化学和1个生物题作答.不按规定选做者.阅卷时将根据所选科目题号的先后顺序只判前面的2个物理题.1个化学题和1个生物题.其他作答的题目答案无效.
网址:http://m.1010jiajiao.com/timu_id_1742473[举报]
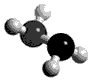
肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池。已知肼的球棍模型如图所示,下列有关说法正确的是
[ ]
A.肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间可形成氢键
C.肼燃烧的热化学方程式为:N2H4(g)+O2(g) = N2(g) +2H2O(g);△H=-642 kJ·mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2+2H2O+4e-=4OH-
查看习题详情和答案>>
B.肼沸点高达l13℃,可推测肼分子间可形成氢键
C.肼燃烧的热化学方程式为:N2H4(g)+O2(g) = N2(g) +2H2O(g);△H=-642 kJ·mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2+2H2O+4e-=4OH-
 肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池.已知肼的球棍模型如图所示,下列有关说法正确的是( )
肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池.已知肼的球棍模型如图所示,下列有关说法正确的是( )
查看习题详情和答案>>
肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池.已知肼的球棍模型如图所示,下列有关说法正确的是( )

查看习题详情和答案>>
| A.肼是由极性键和非极性键构成的非极性分子 |
| B.肼沸点高达l13℃,可推测肼分子间可形成氢键 |
| C.肼燃烧的热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-642 kJ?mol-1 |
| D.肼-氧气燃料电池,负极的电极反应为:O2+2H2O+4e-=4OH- |

肼(N2H4)分子中所示原子均达到稀有气体原子的稳定结构,它的沸点高达l13℃,燃烧热为642kJ?mol-1,肼与氧气及氢氧化钾溶液还可构成燃电池.已知肼的球棍模型如图所示,下列有关说法正确的是( )

A.肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间可形成氢键
C.肼燃烧的热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-642 kJ?mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2+2H2O+4e-=4OH-
查看习题详情和答案>>

A.肼是由极性键和非极性键构成的非极性分子
B.肼沸点高达l13℃,可推测肼分子间可形成氢键
C.肼燃烧的热化学方程式为:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-642 kJ?mol-1
D.肼-氧气燃料电池,负极的电极反应为:O2+2H2O+4e-=4OH-
查看习题详情和答案>>
肼(N2H4)分子中所有原子均达到稀有气体原子的稳定结构,它的沸点高达113℃,燃烧热为642 kJ·mol-1,肼与氧气及氢氧化钾溶液还可构成燃料电池。已知肼的球棍模型如图所示,下列有关说法正确的是( )
| A.肼是由极性键和非极性键构成的非极性分子 |
| B.肼沸点高达l13℃,可推测肼分子间能形成氢键 |
| C.肼燃烧的热化学方程式为:N2H4(g)+ O2(g) = N2(g) +2H2O(g);△H = -642 kJ·mol-1 |
| D.肼-氧气燃料电池,负极的电极反应为:O2 +2H2O+4e-=4OH- |