网址:http://m.1010jiajiao.com/timu_id_1741846[举报]
Ⅰ.称取
Ⅱ.将Ⅰ中所得溶液分成两等份,一份加入酚酞溶液呈红色,用浓度为4.0 mol·L-1?的盐酸中和,用去该盐酸12.5 mL。将另一份用稀硝酸酸化,无气体产生,再加入过量的Ba(NO3)2溶液,得白色沉淀,质量为
Ⅲ.将Ⅰ中所得的
(1)定性分析:由上述实验现象(不进行数据的计算)可以确定该粉末中一定不含有的是__________;一定含有的是__________。
(2)定量计算:为了进一步确定该粉末中其他成分是否存在,该同学又对有关数据进行了处理,并最终得出混合物的组成和各成分的物质的量,请写出他的计算过程。
查看习题详情和答案>>某样品为 、
、 固体混合物.拟将一定质量的样品与稀硫酸反应,用测出生成
固体混合物.拟将一定质量的样品与稀硫酸反应,用测出生成 体积的方法计算出样品中组分的质量分数.为较准确地测出生成的
体积的方法计算出样品中组分的质量分数.为较准确地测出生成的 的体积,在反应结束后加热反应混合液,使溶于溶液的
的体积,在反应结束后加热反应混合液,使溶于溶液的 逸出,待冷却后再测
逸出,待冷却后再测 的体积.(加热时蒸发的水的体积不计)
的体积.(加热时蒸发的水的体积不计)
下面是实验装置,其中B和C可供选择(B、C中所盛的液体为饱和 溶液).
溶液).
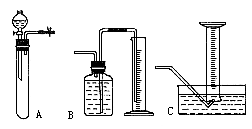
(1)用托盘天平称取样品W g,若所用天平游码的最大刻度为5 g,则与此天平配套的砝码中最小的质量是________(选填编码:A.1 g;B.2 g;C.3 g;D.5 g;E.10 g)
(2)对A进行气密性检查的最简单的方法是________.
(3)已知所用硫酸的浓度为0.5 mol/L,A中试管的规格是20 mm(内径)×200 mm(高度),则在称取样品时,W的值应不大于________ g.测定气体体积所用量筒的规格,合适的是________(A.100 mL;B.200 mL;C.500 mL).
(4)测量 气体的体积时,可选用B、C中的一种与A连接,你将选择(填“B”或“C”),不选另一种的理由是________.
气体的体积时,可选用B、C中的一种与A连接,你将选择(填“B”或“C”),不选另一种的理由是________.
N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
①在该温度时,取l mol N2和3mol H2放在密闭容器中,在催化剂存在下进行反应,测得反应放出的热量总是
②一定条件下,上述可逆反应在体积固定的密闭容器中进行,下列叙述能说明反应已达到平衡的是
A.NH3生成的速率与NH3分解的速率相等
B.混合气体的反应速率
| 2 |
| 3 |
C.容器内的密度不再变化
D.单位时间内消耗a mol N2,同时生成2a mol NH3
(2)25℃时,将工业生产中产生的NH3溶于水得0.1mol/L氨水20.0mL,测得PH=11,则该条件下,NH3?H2O的电离平衡常数为
c(N
| ||
| c(OH-) |
(3)常温下,向0.001mol/LAlCl3溶液中通入NH3直至过量,当pH=