摘要:23.下列通入的气体在化学反应中既作氧化剂又作还原剂的是 ( ) A.SO2通入水中 B.NO2通入水中 C.CO2通入Na2O2中 D.CO 通入灼热的CuO中
网址:http://m.1010jiajiao.com/timu_id_1741590[举报]
下列说法正确的是
A.浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂
B.在任何条件下都不能发生Cu+H2SO4=CuSO4+H2 反应
反应
C.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应
D.二氧化氮与水反应的离子方程式是3NO2+H2O=2HNO3+NO
查看习题详情和答案>>
下列说法正确的是
| A.浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂 |
B.在任何条件下都不能发生Cu+H2SO4=CuSO4+H2 反应 反应 |
| C.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应 |
| D.二氧化氮与水反应的离子方程式是3NO2+H2O=2HNO3+NO |
下列说法正确的是
| A.浓盐酸在化学反应中既可以做氧化剂,又可以作还原剂 |
B.在任何条件下都不能发生Cu+H2SO4=CuSO4+H2 反应 反应 |
| C.浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气都首先发生置换反应 |
| D.二氧化氮与水反应的离子方程式是3NO2+H2O=2HNO3+NO |
二氧化碳作为未来碳源,既可弥补因石油、天然气等大量消耗引起的“碳源危机”,又可有效地解决温室效应.目前,人们利用光能和催化剂,可将CO2和H2O(g)转化为CH4和O2.某研究小组选用不同的催化剂(a,b,c),获得的实验结果如图1所示.
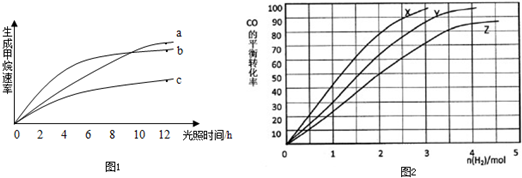
请回答下列问题:
(1)反应开始后的12小时内,在 (填a、b、c)的作用下,收集CH4的最多.
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206kJ?mol-1.将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应5min后达到平衡,此时测得CO的物质的量为0.10mol,则5min内CH4的平均反应速率为 .平衡后可以采取下列 的措施能使 n(CO)/n(CH4)增大.
A.加热升高温度 B.恒温恒容下充入氦气
C.恒温下增大容器体积 D.恒温恒容下再充入等物质的量的CH4和H2O
(3)该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH(l)、H2(g)的燃烧热△H分别为-283.0kJ?mol-1、-726.5kJ?mol-1和-285.8kJ?mol-1,则CO(g)和H2(g)合成CH3OH(l)的热化学方程式为 .
(4)某科研人员为研究H2和CO合成甲醇的最佳起始组成比n(H2):n(CO),在1L恒容密闭容器中通入H2与CO的混合气(CO的投入量均为1mol),分别在230℃、250℃和270℃进行试验,测得结果如图2,则230℃时的实验结果所对应的曲线是 (填字母);理由是 .列式计算270℃时该反应的平衡常数K: .
查看习题详情和答案>>

请回答下列问题:
(1)反应开始后的12小时内,在
(2)将所得CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+206kJ?mol-1.将等物质的量的CH4和H2O(g)充入1L恒容密闭容器,某温度下反应5min后达到平衡,此时测得CO的物质的量为0.10mol,则5min内CH4的平均反应速率为
A.加热升高温度 B.恒温恒容下充入氦气
C.恒温下增大容器体积 D.恒温恒容下再充入等物质的量的CH4和H2O
(3)该反应产生的CO和H2可用来合成可再生能源甲醇,已知CO(g)、CH3OH(l)、H2(g)的燃烧热△H分别为-283.0kJ?mol-1、-726.5kJ?mol-1和-285.8kJ?mol-1,则CO(g)和H2(g)合成CH3OH(l)的热化学方程式为
(4)某科研人员为研究H2和CO合成甲醇的最佳起始组成比n(H2):n(CO),在1L恒容密闭容器中通入H2与CO的混合气(CO的投入量均为1mol),分别在230℃、250℃和270℃进行试验,测得结果如图2,则230℃时的实验结果所对应的曲线是