摘要:19.下列说法正确的是 ( ) A.向pH=3的HX酸与pH=11的YOH碱等体积混合.所得溶液的pH一定为7 B.在0.1 mol/L (NH4)2Fe(SO4)2溶液中c(H+) + c(NH4+) + c(Fe2+) = c(OH-) + c(SO42-) C.在醋酸钠溶液中c(Na+) >c(CH3COO-)>c(H+)>c(OH-) D.0.2 mol/L HCl与0.1 mol/L NaAlO2等体积混合.所得溶液中 c(Cl-)> c(Na+)>c(Al3+)>c(H+)>c(OH-)
网址:http://m.1010jiajiao.com/timu_id_1740668[举报]
下列说法正确的是( )
A、pH=7的溶液一定显中性
B、pH=6的溶液一定显酸性
C、c(H+)<c(OH-)的溶液一定显碱性
D、c(OH-)=1×10-6 mol/L的溶液一定显酸性
查看习题详情和答案>>
用下图Ⅰ所示装置通电10分钟后,去掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升.下列说法正确的是
( )
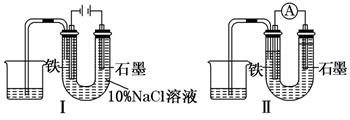
A.同温、同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多
B.用装置Ⅱ进行实验时铁电极的电极反应为Fe-2e- + 2OH- === Fe(OH)2
C.用装置Ⅱ进行实验时石墨电极的电极反应为2H++2e- === H2↑
D.装置Ⅰ通电10分钟后铁电极周围溶液pH降低
查看习题详情和答案>>
在相同温度下,100mL 0.1mol·L-1的醋酸与10mL 1mol·L-1的醋酸相比较,下列说法正确的是( )
| A.发生中和反应时所需NaOH的量前者大于后者 |
| B.前者的电离程度小于后者 |
| C.所含H+的物质的量前者大于后者 |
| D.所含CH3COOH的物质的量前者大于后者 |
下列说法正确的是
| A.由H原子形成1molH—H键要吸收热量 |
| B.化学变化中的能量变化的大小与反应物的质量多少无关 |
| C.酸与碱的稀溶液发生中和反应生成1molH2O时所释放的热量称为中和热 |
| D.锌锰干电池中碳棒是负极,锌片是正极 |