摘要:(2)Cl2 + 2OH-= Cl- + ClO- + H2O
网址:http://m.1010jiajiao.com/timu_id_173764[举报]
(2012?湖南一模)“84消毒液”与硫酸溶液反应可以制取氯气(NaClO+NaCl+H2SO4═Na2SO4+Cl2↑+H2O)为探究氯气的性质,某同学利用此原理制氯气并设计了如图1所示的实验装置.
请回答:
(1)从图2装置中选择合适的制气装置(A处)
(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是
(3)为了验证氯气的氧化性,将氯气通Na2SO3溶液中,写出氯气与Na2SO3溶液反应的离子方程式
(4)氯气通入饱和NaHCO3溶液能产生无色气体,已知酸性盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有
查看习题详情和答案>>

请回答:
(1)从图2装置中选择合适的制气装置(A处)
②
②
(填写序号).(2)装置B、C中依次放的是干燥的红色布条和湿润的红色布条,实验过程中该同学发现装置B中的布条也褪色,其原因可能是
产生的氯气中含有水蒸气会反应生成次氯酸
产生的氯气中含有水蒸气会反应生成次氯酸
,说明该装置存在明显的缺陷,请提出合理的改进的方法在装置A、B之间增加盛有浓硫酸的洗气瓶(或干燥装置)
在装置A、B之间增加盛有浓硫酸的洗气瓶(或干燥装置)
.(3)为了验证氯气的氧化性,将氯气通Na2SO3溶液中,写出氯气与Na2SO3溶液反应的离子方程式
Cl2+SO32-+H2O=SO42-+2Cl-+2H+
Cl2+SO32-+H2O=SO42-+2Cl-+2H+
.(4)氯气通入饱和NaHCO3溶液能产生无色气体,已知酸性盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有
HCl(或盐酸)
HCl(或盐酸)
.某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系).
请你帮助该同学整理并完成实验报告.
(1)实验目的:研究
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等.仪器:①试管,②烧杯,③
(3)实验内容:(填写与实验步骤对应的实验现象的编号)
步骤②③⑤的离子方程式
(4)实验结论:
查看习题详情和答案>>
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②向新制得的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀. |
(1)实验目的:研究
同周期
同周期
元素性质递变规律.(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlCl3溶液,NaOH溶液,酚酞溶液等.仪器:①试管,②烧杯,③
酒精灯
酒精灯
,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等.(3)实验内容:(填写与实验步骤对应的实验现象的编号)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) | B B |
F | A | C C |
D D |
E |
S2-+Cl2=2Cl-+S↓
S2-+Cl2=2Cl-+S↓
,2Na+2H2O=2Na++2OH-+H2↑
2Na+2H2O=2Na++2OH-+H2↑
,2Al+6H+=2Al3++3H2↑
2Al+6H+=2Al3++3H2↑
.(4)实验结论:
同一周期,随着原子序数的递增,元素的金属性逐渐减弱,非金属性逐渐增强
同一周期,随着原子序数的递增,元素的金属性逐渐减弱,非金属性逐渐增强
.根据(1)Fe+Cu2+=Fe2++Cu(2)2Fe3++Cu=Cu2++2Fe2+(3)2Fe2++Cl2=2Fe3++2Cl-(4)HClO+H++Cl-=H2O+Cl2,可以判断出各粒子的氧化性由强到弱的顺序正确的是( )
查看习题详情和答案>>
写出下列反应的离子方程式:
(1)过氧化钠溶于水
(2)苏打溶液中滴入少量盐酸
(3)MnO2与浓盐酸共热
(4)向NaHSO4溶液中逐滴加入Ba (OH)2溶液至溶液呈中性
查看习题详情和答案>>
(1)过氧化钠溶于水
2Na2O2+2H2O═4Na++4OH-+O2↑
2Na2O2+2H2O═4Na++4OH-+O2↑
;(2)苏打溶液中滴入少量盐酸
CO32-+H+═HCO3-
CO32-+H+═HCO3-
;(3)MnO2与浓盐酸共热
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
| ||
MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O
;
| ||
(4)向NaHSO4溶液中逐滴加入Ba (OH)2溶液至溶液呈中性
2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O
2H++2OH-+Ba2++SO42-═BaSO4↓+2H2O
;在以上中性溶液中,继续滴加Ba(OH)2溶液Ba2++SO42-═BaSO4↓
Ba2++SO42-═BaSO4↓
.(一)括号中的物质是杂质,写出除去这些杂质的试剂:
(1)MgO (Al2O3)
(3)FeCl3(FeCl2)
(二)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图1所示:
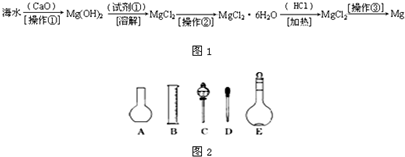
回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式
操作①主要是指
(三)实验室配制480ml 0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体
(2)如图2所示的仪器配制溶液肯定不需要的是
(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
(6)若实验时遇到下列情况,将使溶液的浓度偏低的是
A.配制前设有将容量瓶中的水除尽; B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠; D.称量碳酸钠晶体时所用砝码生锈; E.定容时仰视刻度线.
查看习题详情和答案>>
(1)MgO (Al2O3)
NaOH溶液
NaOH溶液
(2)Cl2(HCl)饱和NaCl溶液
饱和NaCl溶液
(3)FeCl3(FeCl2)
氯气或氯水
氯气或氯水
(4)NaHCO3溶液(Na2CO3)CO2
CO2
(二)海水中含有大量的氯化镁,从海水中提取镁的生产流程如图1所示:

回答下列问题:
写出在海水中加入氧化钙生成氢氧化镁的化学方程式
CaO+MgCl2+H2O=Mg(OH)2+CaCl2
CaO+MgCl2+H2O=Mg(OH)2+CaCl2
;操作①主要是指
过滤
过滤
;试剂①可选用HCl
HCl
;操作②是指蒸发浓缩,冷却结晶,过滤
蒸发浓缩,冷却结晶,过滤
;经操作③最终可得金属镁.(三)实验室配制480ml 0.1mol?L-1的Na2CO3溶液,回答下列问题:
(1)应用托盘天平称取十水碳酸钠晶体
14.3
14.3
g.(2)如图2所示的仪器配制溶液肯定不需要的是
AC
AC
(填序号),本实验所需玻璃仪器E规格为500
500
mL.(3)容量瓶上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的
①③⑤
①③⑤
.(填数字符号)(4)配制所需的主要仪器是:a容量瓶、b烧杯、c胶头滴管、d托盘天平,它们在操作过程中使用的前后顺序是
dbac
dbac
.(填写字母,每种仪器只能选择一次)(5)玻璃棒是化学实验中常用的一种玻璃工具,则在配制溶液的过程中玻璃棒共起到了
2
2
种用途.(填写数字)(6)若实验时遇到下列情况,将使溶液的浓度偏低的是
CE
CE
.A.配制前设有将容量瓶中的水除尽; B.碳酸钠失去了部分结晶水;
C.碳酸钠晶体不纯,其中混有氯化钠; D.称量碳酸钠晶体时所用砝码生锈; E.定容时仰视刻度线.