摘要:20.对于反应2Na2O2+2H2O=4NaOH+O2↑下列说法正确的是 ( ) A.反应中Na2O2是氧化剂.H2O是还原剂 B.反应中O2 既是氧化产物又是还原产物 C.反应中水既不是氧化剂.也不是还原剂 D.有1molNa2O2反应.转移电子2mol
网址:http://m.1010jiajiao.com/timu_id_1736786[举报]
对于反应2Na2O2+2H2O=4NaOH+O2↑下列说法正确的是
A.反应中Na2O2是氧化剂,H2O是还原剂
B.反应中O2 既是氧化产物又是还原产物
C.反应中水既不是氧化剂,也不是还原剂
D.有1molNa2O2反应,转移电子2mol
查看习题详情和答案>>|
下列说法正确的是 | |
| [ ] | |
A. |
2Na2O2+2H2O=4NaOH+O2↑,水作氧化剂 |
B. |
对反应Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O其中1 mol氧化剂在反应中得到的电子为10 mol |
C. |
蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
D. |
判断强弱电解质的依据:溶液的导电能力大小 |
对于反应:2Na2O2 + 2H2O === 4NaOH + O2,下列说法中正确的是
[ ]
A.Na2O2是氧化剂,H2O是还原剂
B.Na2O2既是氧化剂,又是还原剂
C.该反应中电子转移的数目为4e-
D.O2既是氧化产物,又是还原产物
查看习题详情和答案>>
B.Na2O2既是氧化剂,又是还原剂
C.该反应中电子转移的数目为4e-
D.O2既是氧化产物,又是还原产物
(08杭州五校月考)下列说法正确的是 ()
A. 2Na2O2+2H2O=4NaOH+O2↑,水作氧化剂
B. 对反应Cu (IO3)2 + 24KI + 12H2SO4 =2CuI↓+13I2 + 12K2SO4 +12H2O 其中 1mol 氧化剂在反应中得到的电子为10mol
C. 蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质
D. 判断强弱电解质的依据:溶液的导电能力大小
查看习题详情和答案>>I.工业上用CO生产燃料甲醇.一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).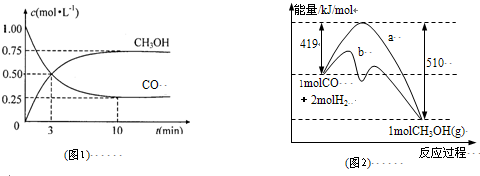
(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是
(3)该反应平衡常数K的表达式为
(4)恒容条件下,下列措施中能使
增大的有
a.升高温度; b.充入He气 c.再充入1molCO和2molH2 d.使用催化剂
II.(13分)某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH.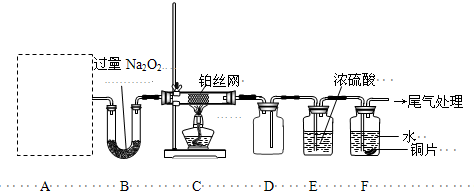
检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
(3)对于C中发生的可逆反应,下列说法正确的是
a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率
c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
查看习题详情和答案>>

(1)图1是反应时CO和CH3OH(g)的浓度随时间变化情况.从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
0.075mol?L-1?min-1
0.075mol?L-1?min-1
;(2)图2表示该反应进行过程中能量的变化.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化.该反应是
放热
放热
(选填“吸热”或“放热”)反应,写出反应的热化学方程式CO(g)+2H2(g)═CH3OH(g)△H=-91KJ/mol
CO(g)+2H2(g)═CH3OH(g)△H=-91KJ/mol
;选择适宜的催化剂,不能
不能
(填“能”或“不能”)改变该反应的反应热;(3)该反应平衡常数K的表达式为
K=
| c(CH3OH) |
| c(CO)×c2(H2) |
K=
,温度升高,平衡常数K| c(CH3OH) |
| c(CO)×c2(H2) |
减小
减小
(填“增大”、“不变”或“减小”);(4)恒容条件下,下列措施中能使
| n(CH3OH) |
| n(CO) |
c
c
.a.升高温度; b.充入He气 c.再充入1molCO和2molH2 d.使用催化剂
II.(13分)某化学课外活动小组设计实验探究氮的化合物的性质,装置如下图所示(A装置未画出),其中A为气体发生装置.A中所用试剂从下列固体物质中选取:a.NH4HCO3、b.NH4Cl、c.Ca(OH)2、d.NaOH.

检查装置气密性后,先将C处铂丝网加热至红热,再将A处产生的气体通过B装置片刻后,撤去C处酒精灯.部分实验现象如下:铂丝继续保持红热,F处铜片逐渐溶解.
(1)实验室制取A中气体时若只用一种试剂,该试剂是
a
a
(填备选试剂的字母);此时A中主要的玻璃仪器有试管、酒精灯(导管)
试管、酒精灯(导管)
(填名称).(2)A中产生的物质被B中Na2O2充分吸收,写出任意一个B中发生反应的化学方程式:
2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2H2O=4NaOH+O2↑或2Na2O2+2CO2=2Na2CO3+O2
.(3)对于C中发生的可逆反应,下列说法正确的是
a
a
.a.增大一种反应物的浓度可以提高另一种反应物的转化率
b.工业上进行该反应时,可采取高压的条件提高反应物转化率

c.该反应在一定条件下达到平衡时,反应物的平衡浓度之比一定是4:5
(4)请在图坐标中画出C装置中反应发生过程中的能量变化示意图,并在虚线上分别标出反应物和生成物的化学式.
(5)待实验结束后,将B中固体混合物溶于500mL1mol?L-1 盐酸中,产生无色混合气体甲,溶液呈中性,则实验前B中原有Na2O2的物质的量是
0.25
0.25
mol,甲在标准状况下是2.8
2.8
L(忽略气体的溶解).