摘要:今有H2.O2.KOH溶液构成燃料电池,则正极通的气体应是 , 负极电极反应式为 . 如把H2改为CH4.还是用KOH作导电解质.则电极反应式分别为 正极: .负极 . 某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息.总的电解反应方程式为:KI+3H2O3=KIO3+3H2↑. (1)椐此推测: ①阳极反应式是 , ②阴极反应式是 . (2)一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源.工业生产1molKIO3.理论上需提供标准状况下的O2 L2.H2 L.
网址:http://m.1010jiajiao.com/timu_id_1736008[举报]
(1)今有H2、O2、KOH溶液构成燃料电池,则正极通的气体应是
(2)
①某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息,总的电解反应方程式为:KI+3H2O=KIO3+3H2↑.椐此推测:阳极反应式是
②一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源,工业生产1molKIO3,理论上需提供标准状况下的O2
查看习题详情和答案>>
O2
O2
,负极电极反应式为H2+2OH--2e-═2H2O
H2+2OH--2e-═2H2O
.如把H2改为CH4,还是用KOH作导电解质,则电极反应式分别为正极:O2+2H2O+4e-═4OH-
O2+2H2O+4e-═4OH-
、负极:CH4+10OH--8e-═CO32-+7H2O
CH4+10OH--8e-═CO32-+7H2O
.(2)
①某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息,总的电解反应方程式为:KI+3H2O=KIO3+3H2↑.椐此推测:阳极反应式是
I--6e-+3H2O═IO-3+6H+
I--6e-+3H2O═IO-3+6H+
;阴极反应式是6H2O+6e-═3H2↑+60H-
6H2O+6e-═3H2↑+60H-
.②一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源,工业生产1molKIO3,理论上需提供标准状况下的O2
33.6
33.6
L,H20
0
L.(1)今有H2、O2、KOH溶液构成燃料电池,则正极通的气体应是______,负极电极反应式为______.如把H2改为CH4,还是用KOH作导电解质,则电极反应式分别为正极:______、负极:______.
(2)
①某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息,总的电解反应方程式为:KI+3H2O=KIO3+3H2↑.椐此推测:阳极反应式是______;阴极反应式是______.
②一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源,工业生产1molKIO3,理论上需提供标准状况下的O2______L,H2______L.
查看习题详情和答案>>
(2)
①某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息,总的电解反应方程式为:KI+3H2O=KIO3+3H2↑.椐此推测:阳极反应式是______;阴极反应式是______.
②一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源,工业生产1molKIO3,理论上需提供标准状况下的O2______L,H2______L.
(1)今有H2、O2、KOH溶液构成燃料电池,则正极通的气体应是______,负极电极反应式为______.如把H2改为CH4,还是用KOH作导电解质,则电极反应式分别为正极:______、负极:______.
(2)
①某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息,总的电解反应方程式为:KI+3H2O=KIO3+3H2↑.椐此推测:阳极反应式是______;阴极反应式是______.
②一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源,工业生产1molKIO3,理论上需提供标准状况下的O2______L,H2______L.
查看习题详情和答案>>
(2)
①某一资料中记载着可以用电解KI水溶液的方法进行KIO3的工业化生产的信息,总的电解反应方程式为:KI+3H2O=KIO3+3H2↑.椐此推测:阳极反应式是______;阴极反应式是______.
②一位学生想用氢氧燃料电池来作电解KI水溶液进行KIO3的工业化生产的电源,工业生产1molKIO3,理论上需提供标准状况下的O2______L,H2______L.
查看习题详情和答案>>
(1)今有2H2+O2
2H2O反应,构成燃料电池,则负极通的应是 ,电极反应式为 ;
(2)如把KOH改为稀H2SO4作电解质溶液,则该电极反应式为 ;(1)和(2)的电解液不同,反应进行后,其溶液的pH各有何变化? ;
(3)如把H2改为甲烷、KOH作导电物质,则电极反应式为: 、 .
查看习题详情和答案>>
| ||
(2)如把KOH改为稀H2SO4作电解质溶液,则该电极反应式为
(3)如把H2改为甲烷、KOH作导电物质,则电极反应式为:
能源是人类生存和发展的重要支柱.研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义.已知下列热化学方程式
①2H2(g)+O2(g)=2H2O(l)△H=-570kJ/mol;
②H2(g)+
O2(g)=H2O(g)△H=-242kJ/mol;
③C(s)+
O2(g)=CO(g)△H=-110.5kJ/moL;
④C(s)+O2(g)=CO2(g)△H=-393.5kJ/moL;
⑤CO2(g)+2H2O(g)=2CH4(g)+2O2(g)△H=+890kJ/moL
回答下列问题
(1)H2的燃烧热为 .
(2)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然难直接测定,但可通过间接的方法求得.已知C(s)+H2O(g)=H2(g)+CO(g)△H=akJ/moL;
则a= ;该反应的熵△S 0(选填“>”、“=”、“<”);已知自由能△G=△H-T△S,当△G<0时可自发进行.则该反应在什么条件下可自发进行 .
(3)事实证明,能设计成原电池的反应通常是放热反应.
①下列化学反应在理论上可以设计成原电池的是 .
A.C(s)+H2O(g)=CO(g)+H2(g)△H>0
B.2H2(g)+O2(g)=2H2O(l)△H<0
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H<0
②以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式为 .
(4)有同学利用CuSO4溶液,进行以下实验探究.
①图一是根据反应Zn+CuSO4=Cu+ZnSO4 设计成的锌铜原电池.
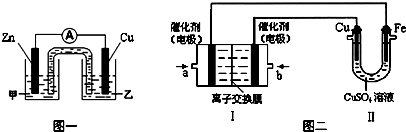
电解质溶液乙是 (填“ZnSO4”或“CuSO4”)溶液;Cu极的电极反应式是 .
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是 (填“CH4”或“O2”),a处电极上发生的电极反应式是 .
查看习题详情和答案>>
①2H2(g)+O2(g)=2H2O(l)△H=-570kJ/mol;
②H2(g)+
| 1 |
| 2 |
③C(s)+
| 1 |
| 2 |
④C(s)+O2(g)=CO2(g)△H=-393.5kJ/moL;
⑤CO2(g)+2H2O(g)=2CH4(g)+2O2(g)△H=+890kJ/moL
回答下列问题
(1)H2的燃烧热为
(2)盖斯定律在生产和科学研究中有很重要的意义.有些反应的反应热虽然难直接测定,但可通过间接的方法求得.已知C(s)+H2O(g)=H2(g)+CO(g)△H=akJ/moL;
则a=
(3)事实证明,能设计成原电池的反应通常是放热反应.
①下列化学反应在理论上可以设计成原电池的是
A.C(s)+H2O(g)=CO(g)+H2(g)△H>0
B.2H2(g)+O2(g)=2H2O(l)△H<0
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H<0
②以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式为
(4)有同学利用CuSO4溶液,进行以下实验探究.
①图一是根据反应Zn+CuSO4=Cu+ZnSO4 设计成的锌铜原电池.

电解质溶液乙是
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是